解构“妖股”通化金马
每经记者 林姿辰 每经编辑 杨夏
7月2日,美国食品药品监督管理局(FDA)批准Kisunla(Donanemab),礼来制药的阿尔茨海默病疗法用于治疗成人早期症状性阿尔茨海默病(AD)。
全球各大药企在阿尔茨海默病新药研发领域折戟早已成为“常态”,美国药物生产与研发协会数据显示,全球累计在AD上的研发投入超过6000亿美元,失败的临床药物超过300种,失败率高达99.6%。
因此,阿尔兹海默症的药物也被称为“研发坟场”。但在去年,当一家东北药企――通化金马(000766.SZ,股价16.29元,市值157.44亿元)宣布20年前的“老方子”完成三期临床试验时,公司股价一飞冲天,在A股市场博得不少关注。但在六月中旬,《每日经济新闻》记者前往通化金马年度股东大会,发现现场只有几名个人股东参会。
事后,从北京跨越千里赶来参加大会的丁先生对记者表示了自己的惊讶,“像我这样的投资者应该是很多的,怎么基本没人去(股东大会)?市场对这个事情是不是太冷淡了,这么开天辟地的一件事情,甚至没有机构投资者去他们公司调研?”
7月3日,《每日经济新闻》记者向通化金马方面发送采访邮件;6天后,公司方面回复称相关人员目前都很忙,过一段时间将安排人员接受采访,但截至发稿记者未获进一步联系。

炙手可热的股价与门可罗雀的股东大会
股价在短短3个多月内涨超260%,又在一天内闪崩跌停,2023年12月12日俨然成为通化金马热度的分界线。截至目前,公司的股价已经回落至8元左右,但市值依然是去年8月的3倍,涨幅在医药股中“遥遥领先”。
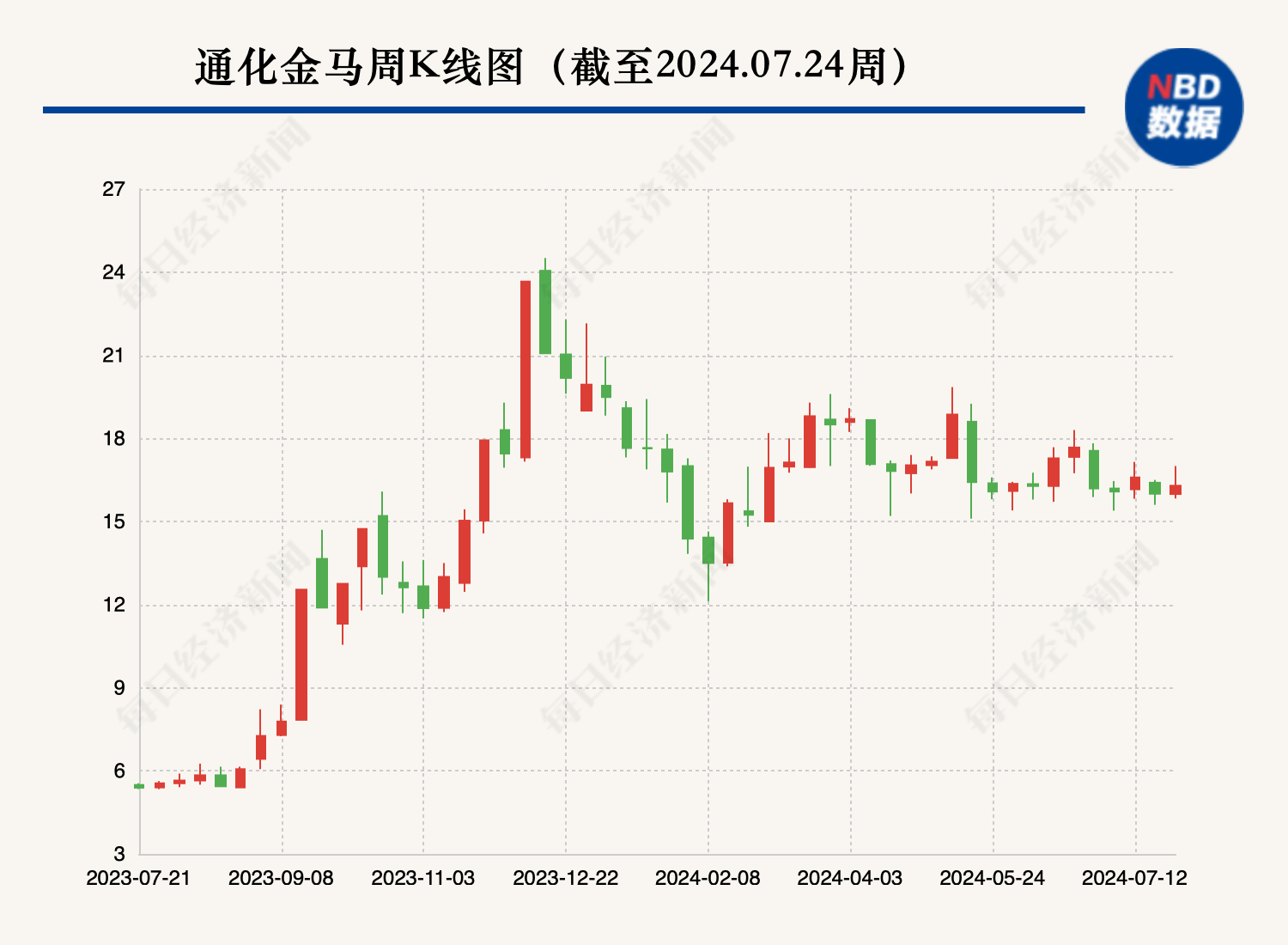
这家上市于1997年的药企在一夜之间被贴上“妖股”的标签,与阿尔兹海默症有关。在资本市场中,AD是医药股“一点就燃”的概念,而引爆通化金马的是琥珀八氢氨吖啶片Ⅲ期临床试验进度。
据介绍,琥珀八氢氨吖啶片是具备完全自主知识产权的小分子化学I.I类国家级新药,目前已获得日本、欧盟专利,是国家十三五重大新药创制项目。这种口服固体制剂主要用于治疗轻、中度阿尔茨海默病,是一种新的乙酰胆碱酯酶抑制剂,具有双重胆碱酯酶抑制功能,可以同时抑制乙酰胆碱酯酶和丁酰胆碱酯酶。
2023年8月24日,通化金马在官微宣布琥珀八氢氨吖啶片的盲态数据审核会如期举行,8月30日至9月18日,公司股价从6.17元涨至13.52元,区间涨幅达119.12%。9月20日,公司股价出现一字跌停,但随着公司公告称琥珀八氢氨吖啶片Ⅲ期临床试验达到主要临床试验终点,股价在9月21日又迎来涨停,上涨趋势一直延续到12月。
目前,通化金马市值仍超过150亿元,但前十大股东持股占比从去年6月底的51.54%下降到今年一季度末的38.83%。其中,原第二大股东上海木恺贸易有限公司在去年第四季度减持3000万股,截至今年一季度末,在以1.84%的持股比例位列第七大股东。
重要股东高位减持的同时,通化金马也并未受到太多专业机构关注。在可查询的定期公告的披露中,机构投资者只持有少量通化金马股份,2023年年报显示,9家基金公司合计持有通化金马不足1%股份。
另外,券商研报也鲜少覆盖通化金马。Wind显示,通化金马上一份覆盖研报的发布时间还停留在2018年,近5年没有机构覆盖。
而公司披露重磅产品进展后的首场年度股东大会现场也非常冷清。
 通化金马 图片来源:每经记者 林姿辰 摄
通化金马 图片来源:每经记者 林姿辰 摄在今年6月的2023年年度股东大会上,董事长线上参会、到场的外部股东只有两三名,没有机构投资者参与。公司在走完常规流程后,股东大会便结束收场。
丁先生是通化金马股东大会首位到会的外部股东。他告诉记者,自己从2023年8月开始关注通化金马,之后不断加仓,看重的就是琥珀八氢氨吖啶片这款药。
但通化金马股东大会现场的“冷清”,多少让丁先生感到意外,他觉得琥珀八氢氨吖啶片是一款阿尔茨海默症领域的开创性药物,无论是疗效还是技术都处于全球领先水平,如果能顺利注册并推向市场,“真的是放卫星,全球第一了”。
“体外试验表明,琥珀八氢氨吖啶片对乙、丁两种胆碱酯酶的抑制能力分别是常规一线用药的数倍,故有更好的临床治疗效果,同时I期、II期临床也验证了其临床效果;并且,琥珀八氢氨吖啶片的安全性相对更可靠、更安全。”丁先生认为,这是一个稀缺标的,因为阿尔茨海默症目前还没有有效的治疗药物。
通过与公司高管的线下交流,丁先生对琥珀八氢氨吖啶片持有信心,认为“药物上市后的年纯利润预计在十亿元级别以上”,但他最大的顾虑还是公司能否顺利地完成药物注册并将其推向市场。
“短期内我可能不会再购入股票了。”丁先生说。
琥珀八氢氨吖啶片研发进度是否属于重大事项?
创新药领域素来以成败论英雄,但医药研发九死一生,跨国公司因为药物临床不达预期而终止临床试验是常有的事。从通化金马现有的产品管线来看,琥珀八氢氨吖啶片是公司最重视的产品,也是目前百亿元市值的核心溢价部分。
丁先生对琥珀八氢氨吖啶片的这些认知,主要来自公开信息。根据《每日经济新闻》记者在通化金马公众号上梳理,通化金马围绕琥珀八氢氨吖啶片的信息披露动作非常频繁。
2023年8月20日,通化金马在公众号发布关于举行琥珀八氢氨吖啶片盲态数据审核会的问诊,但直到8月31日才发布公告,晚了10天;9月19日公众号发布揭盲发布会的文章,上市公司9月21日发布。而公众号后续发布的一系列进展,却没有出现在上市公司的公告中。

但这些未出现在上市公司公告的信息,却牵动着通化金马的股价。2023年9月1日、13日、15日,通化金马连发股票交易异动公告。11月20日,通化金马举行琥珀八氢氨吖啶片注册工作推进会,11月27日、12月6日发布股票交易异动公告。
记者从与公司有过交流的投资者处了解到,公司认为公告有披露的标准,达不到公告要求不能发布,这些内容属于工作动态,没有涉及重大事项,在公众号发布是正常工作。
但这与行业惯例有些出入,由于Ⅲ期临床试验对于一款创新药的上市至关重要,公开详细的临床试验信息是上市公司更常见的做法,内容一般覆盖试验设计、受试者信息、主要终点和次要终点、安全性数据、疗效数据、统计分析结果等。
例如,2022年8月1日和2日,恒瑞医药分别在公告和微信公众号中披露了创新药吡咯替尼一线治疗乳腺癌的Ⅲ期临床研究数据,关键信息包括“按照1∶1随机入组”“共入组590例受试者”“评价马来酸吡咯替尼片联合曲妥珠单抗和多西他赛对比安慰剂联合曲妥珠单抗和多西他赛一线治疗HER2阳性复发/转移性乳腺癌”“主要研究重点”“次要终点”等。
跨国药企的披露甚至更加详细。以阿尔茨海默病药物刚被FDA批准的礼来举例,2023年7月17日,公司在公布3期临床试验TRAILBLAZER-ALZ 2的完整结果时,明确提到“亚群分析显示,处于疾病最早阶段的受试者获益更为显著,与安慰剂相比,其认知与功能下降减缓达60%”。
相比之下,通化金马于2023年9月20日披露的药物Ⅲ期临床试验揭盲结果非常简单。公司表示,琥珀八氢氨吖啶片治疗轻中度阿尔茨海默病的26周双盲、双模拟、随机、安慰剂/阳性药平行对照暨延至54周单臂、多中心III期临床试验研究于2017年1月,以上海精神卫生中心为组长单位,在全国34家临床试验中心开展相应的临床试验研究。
琥珀八氢氨吖啶片Ⅲ期临床试验达到主要临床试验终点,试验呈阳性结果,认为试验药物对ADAS-cog(阿尔茨海默病评估量表-认知量表)的改善具有明显的临床意义;在安全性上,试验药物的不良事件及不良反应的发生率均低于两个对照组。与安慰剂组比较,结果具有显著的统计学意义,P<0.001。
值得一提的是,三期临床揭盲结果的更多数据,公司是在公众号上披露的。在“通化金马药业”微信公众号2023年12月14日发布的消息中,公司披露了药物有效性和安全性的更详细数据。值得注意的是,此次公司披露了吖啶片组、安慰剂组、阳性药组间的显著统计学意义P值,仍未公布受试者人数、性别等信息,阳性药组的患者使用的哪款药物目前仍未可知。
被质疑伪创新 专家:公开披露的临床结果表述含糊
阿尔茨海默症的竞争市场非常激烈,被称为医药界的“天坑”。也正因为研发难度大,每个药物进展都会引起业内广泛讨论。

 通化金马在其公众号披露的试验数据。 图片来源:“通化金马药业”微信公众号
通化金马在其公众号披露的试验数据。 图片来源:“通化金马药业”微信公众号6月21日,中国老年保健协会阿尔茨海默病分会(ADC)常务副主任委员兼秘书长、北京大学第一医院主任医师孙永安接受《每日经济新闻》记者采访。他表示,上图中针对“主要疗效指标ADAS-cog”的表述有些“含糊”,从所披露的数据看,仅表示“三组间差异具有显著统计学意义”,并没有明说吖啶片组与安慰剂组、吖啶片组与阳性药组之间的是否有差距,谁优谁劣。
而在次要疗效指标CIBIC-plus(临床印象变化量表)和ADCS-ADL(日常生活活动量表)中,数据显示琥珀八氢氨吖啶片对于阿尔茨海默病症状的缓解效果优于安慰剂组,同样未对吖啶片组和阳性药组作比较。
“这些资料不是太全。”孙永安表示,按理说企业应该提供实验组与对照组间的比较数据,并在临床试验入组时披露各组使用药物的情况,否则临床试验数据很容易被质疑。
根据公开信息,截至2023年12月13日,关于琥珀八氢氨吖啶片的统计报告、临床研究总结报告已正式完成定稿。但根据通化金马近期在投资者互动平台的发声,目前仍未向CDE(国家药品监督管理局药品审评中心)提交新药上市申请,考虑到速度最快的“绿色通道”预计审批时间为6个月到1年,琥珀八氢氨吖啶片很难在2024年前获批上市。
通化金马被质疑的另一个原因,在于其在研药物并非真正的原始创新。
阿尔茨海默病致病机制复杂,存在着等多种假说,其中胆碱能假说是最早提出的解说,对应的药物数量也最多。现阶段治疗阿尔茨海默病的中国市场常用药物包括胆碱酯酶抑制剂(如多奈哌齐、卡巴拉汀、加兰他敏和石杉碱甲)和兴奋性氨基酸受体拮抗剂(如盐酸美金刚)。
 目前已获得FDA批准上市的阿尔茨海默病疗法。 图片来源:中国银河证券研究院
目前已获得FDA批准上市的阿尔茨海默病疗法。 图片来源:中国银河证券研究院孙永安表示,在阿尔茨海默病领域,胆碱酯酶抑制剂是一种经典药物。例如,日本卫材公司的多奈哌齐于1996年获美国FDA的特许批准用于临床,诺华公司的卡巴拉汀则于1997年在瑞士上市。其中,后者能同时抑制乙酰胆碱酯酶和丁酰胆碱酯酶,均能改善阿尔茨海默病病人的认知作用更优。
目前,国内已有北京四环制药、浙江京新药业、国药集团国瑞药业、安徽泰恩康制药拥有重酒石酸卡巴拉汀胶囊的批文,均已过评。除了胶囊剂外,国内还获批了片剂(仿制)和透皮贴剂。原研还有口服液剂型,并未在国内上市,不过,国内已有浙江赛默制药、百善科技(湖州)、山东朗诺制药、呋欧医药科技(湖州)4家企业报产。
孙永安告诉记者,该类药物的临床效果只能在一定时间窗内改善患者症状,无法从根本上改变疾病病程。因此,与卡巴拉汀作用机理相同的琥珀八氢氨吖啶片,其疗效不可能是颠覆性的,并非业内常说的“first in class”(首创药物)而更像是me-better(在仿制中创新的药物)。
首先,琥珀八氢氨吖啶片对乙、丁两种胆碱酯酶的抑制能力分别是常规一线用药的数倍,并不意味着其对阿尔茨海默病患者的症状缓解效果就是其他药物的数倍。这是因为,虽然胆碱酯酶抑制剂可以通过延缓胆碱能神经元对释放的乙酰胆碱的降解,促进胆碱能神经传导并改善胆碱能介导的认知功能障碍,但引发认知功能障碍的因素还有很多,比如细胞毒性破坏神经细胞、线粒体代谢障碍、血管性损伤因素、慢性炎症等,因此乙酰胆碱的含量与认知功能不完全成正比。
而且,胆碱酯酶抑制剂本身“治标不治本”。孙永安举了一个很形象的比喻,肺部感染是细菌感染引起的炎症,用抗生素把细菌给杀死是肺部感染的根本治疗,帮助咳痰、降温的药物主要是改善肺部感染症状,同样道理,胆碱酯酶抑制剂只是改善认知症状,对疾病本身的进展并没有太大帮助,在阿尔茨海默病的治疗中,胆碱酯酶抑制剂发挥的作用就像降温药一样。
因此,尽管通化金马表示,在过去的十几年里,胆碱酯酶抑制剂领域一直无新的原研药品上市,“公司经过近二十年的研发,在该疾病用药领域有了较大突破”。但值得注意的是,近年来,针对疾病致病因素的单抗陆续获批上市,为针对该病的病因进行治疗提供了可能,全球性药企逐渐转向了疾病修饰治疗领域。
6月20日,一位业内知名投资人士也对《每日经济新闻》记者表示,自己不认为琥珀八氢氨吖啶片是一个革命性的药物,它与很多跨国药企正在研究的单抗药物不可同日而语。
未来,公司能否凭借琥珀八氢氨吖啶片的“幸运”破局?答案尚未揭晓,但留给通化金马的证明时间不多了。
