华东医药创新药布局里程碑,First-in-Class自免新药国内BLA已获受理
11月13日,华东医药(000963.SZ)发布公告称,全资子公司杭州中美华东制药有限公司(以下简称“中美华东”)从美国Kiniksa公司引入的注射用利纳西普(ARCALYST,Rilonacept)上市申请获得国家药品监督管理局(NMPA)正式受理,用于治疗成人和12岁及以上儿童的冷吡啉相关的周期性综合征 (CAPS),包括家族性寒冷型自身炎症综合征(FCAS)和穆-韦二氏综合征(MWS)。ARCALYST治疗CAPS适应症在国内被列入临床急需境外新药目录,同时是美国FDA批准的唯一一款适用于12岁及以上人群的治疗复发性心包炎药物,是首创新药(First-in-Class)。
新药填补治疗空白,罕见病市场潜力巨大
公告显示,ARCALYST是重组二聚体融合蛋白,可阻断白细胞介素-1α(IL-1α)和白细胞介素-1β(IL-1β)的信号传导,于2008年获得美国食品和药物管理局(FDA)批准,用于治疗CAPS、FCAS和MWS。2020年,FDA批准其用于治疗IL-1受体拮抗剂缺乏症(DIRA)。中美华东于2022年2月获得全球性生物制药公司Kiniksa的ARCALYST的独家许可。因冷吡啉相关的周期性综合征是罕见病且在中国目前无有效治疗药物,2018年,注射用利纳西普被纳入国家药品监督管理局药品审评中心(CDE)发布的《临床急需境外新药名单(第一批)》。
ARCALYST的引进不仅有望转变国内CAPS患者的治疗模式,更能够对复发性心包炎产生卓越的疗效。2019年,FDA授予ARCALYST治疗复发性心包炎突破性疗法认定,2021年,ARCALYST获FDA批准用于治疗复发性心包炎。心包炎是心包疾病的最常见形式,主要影响心脏周围组织的炎症性心血管疾病,其中,约30%的心包炎患者会经历复发,成为复发性心包炎。复发性心包炎是一种失能性疾病,患者会有反复的胸痛发作,严重时可能危及生命。目前,针对复发性心包炎的标准疗法较少,且副作用较大,临床治疗存在未满足的需求。ARCALYST是美国FDA批准的唯一一款适用于12岁及以上人群的治疗复发性心包炎药物,2023年6月底华东医药已完成复发性心包炎适应症的中国Pre-BLA递交。
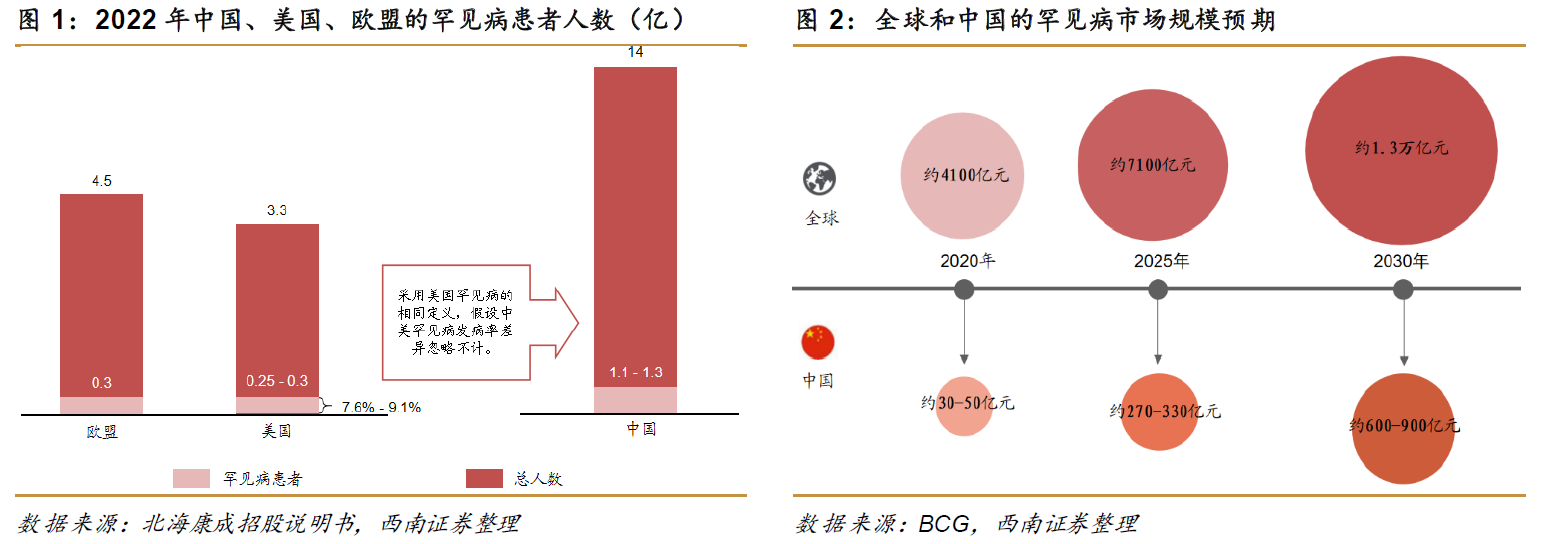
值得一提的是,CAPS和复发性心包炎都是罕见病,而中国是罕见病的单一最大市场,存在较大的市场潜力。由于患病率较低,开发罕见病药物的制药公司相对较少,因此存在较大的市场空白。据《2022中国罕见病行业趋势观察报告》统计,2022 年中国罕见病患者约2000万,而目前国内被认定的罕见病种类仅为131种,远低于美国和欧盟认定的罕见病种类(均多于6000种),还有大部分的罕见病并未被目录收归其中。公开数据显示,根据欧盟和美国对罕见病的广泛定义,中国患有一种或多种罕见病患者可能超过1亿,潜在罕见病患者人数大概为美国的4倍以上。
国内存在大量未被满足的患病群体,罕见病市场存在较大的市场增长空间。2020年全球罕见病市场规模约为4100亿元,中国市场约30-50 亿元,占比约为1%。根据BCG预测,2030年全球罕见病市场有望达到1.3万亿元,中国罕见病市场份额则有望达到600-900亿元,约占全球市场的5%-7%。
 图片来源:西南证券研报
图片来源:西南证券研报与此同时,ARCALYST海外销售数据持续攀升,获得众多医生和患者的青睐。据Kiniksa公布的2023年三季报,ARCALYST第三季度实现产品销售收入6480万美元,同比大增94.01%。2023年1-9月,产品净收入约为1.62亿美元,据Kiniksa预计,ARCALYST今年全年有望实现销售收入2.2-2.3亿美元,以中值计算相比2022年增长幅度将达到84%。
不难预计,ARCALYST在国内上市后有望复制甚至超越其在海外的成功。ARCALYST在国内注册上市的顺利推进,将为国内罕见病患者带来新的希望,这同时也离不开华东医药近年来在创新药领域的持续深耕。
华东医药创新药持续布局,三大领域协同发力
华东医药创新药坚持差异化研发策略,以全球患者未满足的临床需求为导向,重点布局内分泌、自身免疫及肿瘤三大领域,致力于成为国内这三大产品领域的领跑企业。目前创新产品管线已达到46项,其中自主研发项目达到50%的比例。随着产品管线的不断丰富,公司在创新药领域已持续扩展至包括小分子药物、多肽类药物、抗体药物偶联物(ADC)、双特异性或多特异性抗体药物等更多类型的药物研发,以及针对内分泌、自身免疫及肿瘤等疾病的创新疗法的探索。
近年来,华东医药围绕自身免疫领域不断进行深入布局,引进全球领先的创新技术与产品,同时持续提升自身创新研发能力。截至目前,公司在自免疾病领域已拥有生物药和小分子创新产品10余款。同时,公司创新药研发中心自主开发了多个全新靶点和生物学机制的免疫疾病早期项目,均在顺利推进中。
在自免领域,华东医药现有产品及在研产品适应症涵盖移植免疫、系统性红斑狼疮、银屑病、特应性皮炎、脂溢性皮炎、复发性心包炎、冷吡啉相关的周期性综合征等适应症,覆盖皮肤、风湿、心血管、呼吸、移植等疾病种类,是国内自身免疫性疾病领域种类覆盖较为全面的医药公司之一。
华东医药结合项目实践,搭建了特色外用制剂平台,稳步推进外用制剂、复杂制剂等研发创新,重点包括外用溶液剂、软膏剂、凝胶剂、乳膏剂等项目的开发、提高体外释放和透皮实验方法开发能力、生物药生化检测能力、原料药及中间体杂质谱分析及结构确证水平等。目前公司控股子公司华东医药(西安)博华制药有限公司已建成三条外用制剂生产线。
此外,华东医药自研的乌司奴单抗生物类似药 HDM3001(QX001S)上市许可申请已于 2023 年 8 月获得NMPA受理,用于治疗斑块状银屑病。用于治疗系统性红斑狼疮的创新药 HDM3002(PRV-3279)已正式加入 IIa 期 MRCT试验(PREVAIL-2)。公司自主开发了多个全新靶点和生物学机制的免疫疾病早期项目,均在顺利推进中,今年第四季度自免领域将有 1 款自主创新产品获得 PCC 确认。
在肿瘤领域,华东医药围绕ADC产品重点布局,不断夯实管线,继续保持国内ADC领域优势地位。公司力争打造全球领先的肿瘤创新药物研发平台,通过药物前期开发的新靶点发现、筛选和验证,建立了涵盖靶向小分子化药、ADC、抗体、PROTAC等超过30项肿瘤创新药产品。
华东医药从美国ImmunoGen引进的全球首创ADC新药索米妥昔单抗注射液(ELAHERE)的中国BLA申请已于2023年10月获得受理,该产品已于2023年7月被CDE纳入优先审评品种名单,有望于半年内获批上市。
内分泌领域,华东医药以GLP-1靶点为核心,打造了全球领先的糖尿病创新药物研发平台。目前,公司已建立了涵盖口服、注射剂等多种剂型包括长效和多靶点全球创新药和生物类似药相结合的GLP-1及相关靶点8款产品。未来,公司将继续探索与GLP-1相关靶点的创新项目,拓展减重、降脂、非酒精性脂肪性肝炎(NASH)、心血管获益、慢性肾脏病(CKD)等相关适应症研发工作,持续开发具有迭代性、更具临床优势的创新药物。
华东医药自主研发的口服小分子GLP-1受体激动剂HDM1002糖尿病适应症已于2023年5月首获中美双IND批准,并于2023年6月初实现首例受试者用药(FIH)。肥胖适应症的中国IND申请已于2023年9月获批。截至目前,全球尚无口服小分子GLP-1受体激动剂药物上市,HDM1002将进一步丰富公司在内分泌治疗领域的产品管线,加速公司融入全球创新医药产业的步伐,进一步提升公司综合竞争力。
未来,华东医药将继续通过自主研发、外部合作和产品授权引进等方式,不断优化提升差异化创新产品管线,有效保障持续有创新产品临床推进和上市的良好发展态势,为中长期发展提供源源不断新动能。