哈三联帕拉米韦注射液上市申请获受理,有望切入10亿抗流感市场
(来源:摩熵医药大数据)
8月12日,CDE官网显示,哈尔滨三联药业股份有限公司按3类化药注册申报的帕拉米韦注射液上市申请已获受理。据摩熵医药数据库显示,该药物近两年院内市场销售额超10亿元。
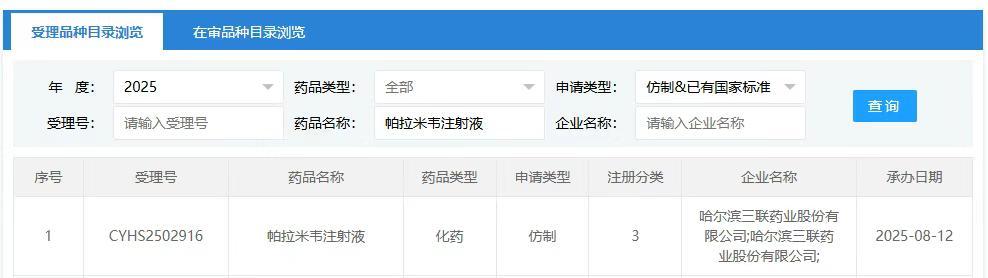 截图来源:CDE官网
截图来源:CDE官网帕拉米韦是新一代神经氨酸酶抑制剂,适用于全年龄段甲型或乙型流行性感冒患者的治疗。该药物由日本盐野义从美国BioCryst公司引进,2010年在日本获批上市,商品名为“Rapiacta”。
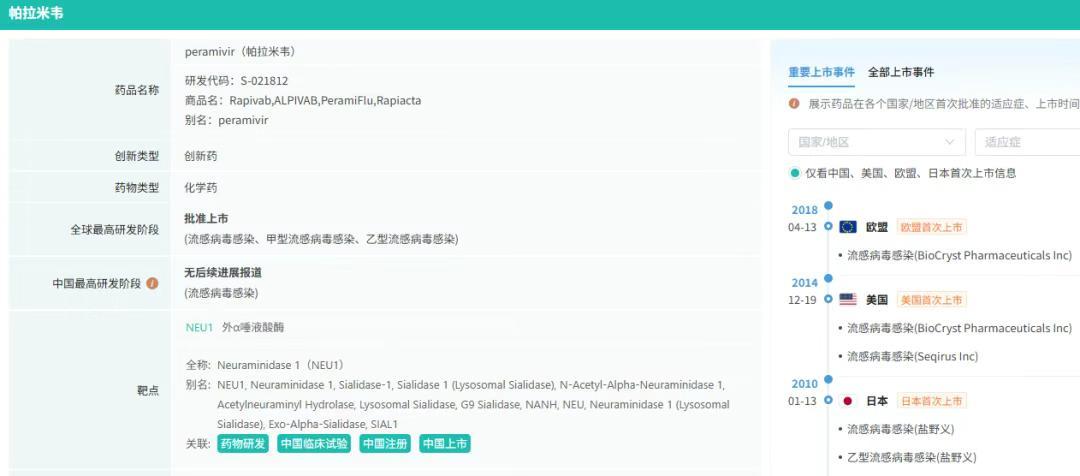 截图来源:摩熵医药全球药物研发数据库
截图来源:摩熵医药全球药物研发数据库2014年12月,帕拉米韦注射液在美国获批上市,是FDA唯一批准的抗流感注射剂,也是继扎那米韦和奥司他韦之后的又一新型流感病毒NA抑制剂。
据摩熵医药数据库显示,2022年帕拉米韦于院内市场斩获5.24亿元销售额,同比增长25.55%;2023年突破10亿大关,实现翻倍式增长。2024年销售额攀升至11.46亿元,处于当前最高水平。
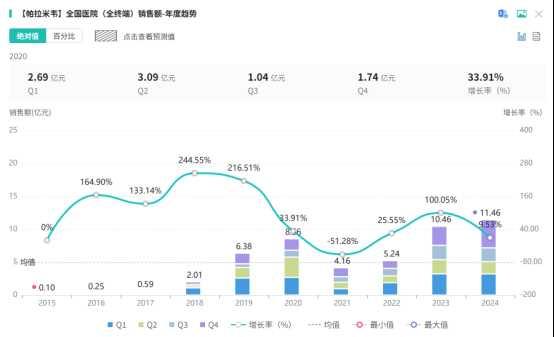 截图来源:摩熵医药全国医院(全终端)销售数据库
截图来源:摩熵医药全国医院(全终端)销售数据库在国内市场帕拉米韦上市剂型涵盖帕拉米韦注射液与帕拉米韦氯化钠注射液。其中,帕拉米韦注射液的生产批文涉及35家企业,包括齐鲁制药、扬子江药业、中国大冢制药、石药集团等;而帕拉米韦氯化钠注射液的生产企业仅有2家,即广州南新制药和山东齐都药业。
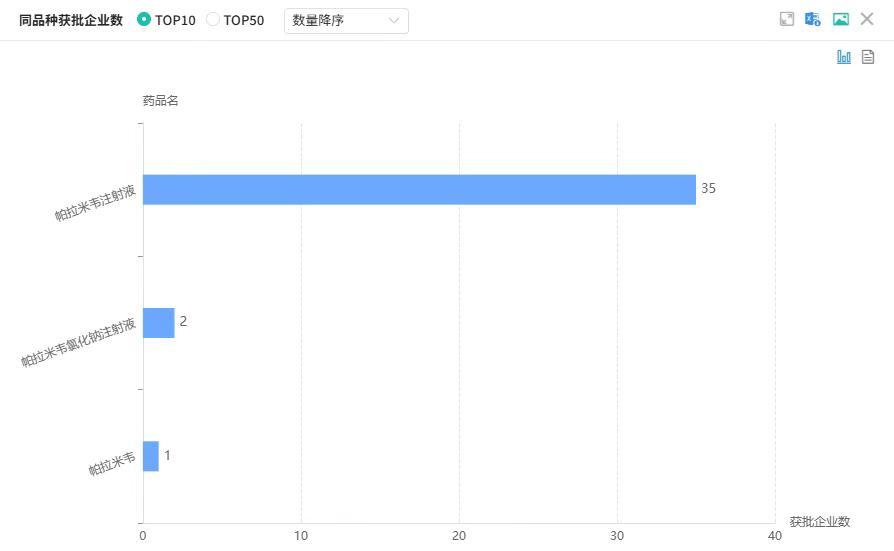 截图来源:摩熵医药中国药品批文数据库
截图来源:摩熵医药中国药品批文数据库2013年,南新制药的帕拉米韦氯化钠注射液在国内获批上市。因原研产品未进入中国市场,该领域长期由南新制药主导。当前,该企业占据帕拉米韦94.49%的市场份额。
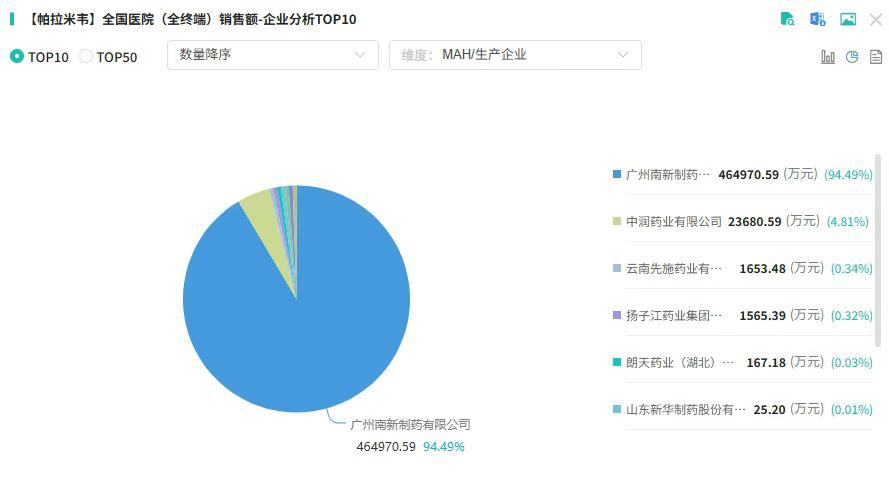 截图来源:摩熵医药全国医院(全终端)销售数据库
截图来源:摩熵医药全国医院(全终端)销售数据库2023年3月,中润药业的帕拉米韦注射液获批上市,成为国内首仿。同年6月,扬子江药业集团四川海蓉药业获批,视同过评,成为国内第二家获得该品种仿制批文的企业。
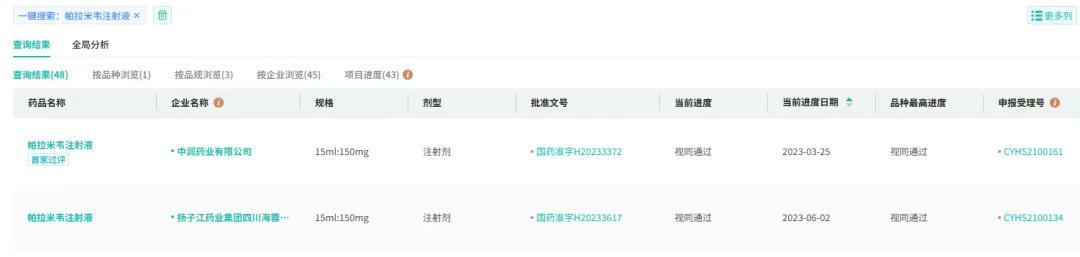 截图来源:摩熵医药一致性评价数据库
截图来源:摩熵医药一致性评价数据库当前还有浙江康吉尔药业、广州一品红制药、山东益康药业等10家企业的帕拉米韦注射液在审评审批中。
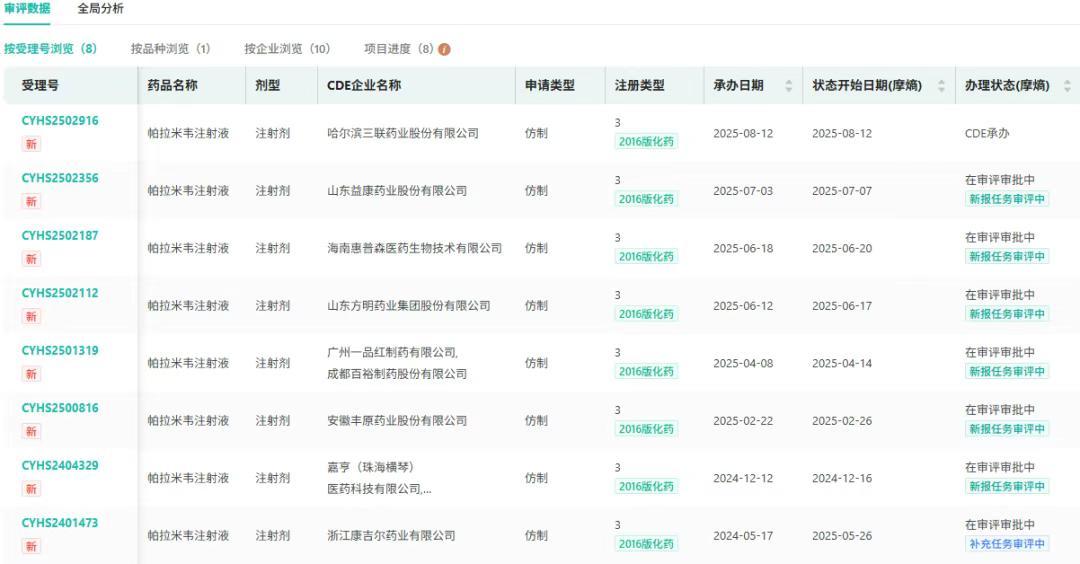 截图来源:摩熵医药中国药品审评数据库
截图来源:摩熵医药中国药品审评数据库摩熵医药数据显示,帕拉米韦原料药目前已有12家企业完成备案流程。其中有10家的产品处于 “A” 状态,即已通过审评,或与制剂成功实现关联。
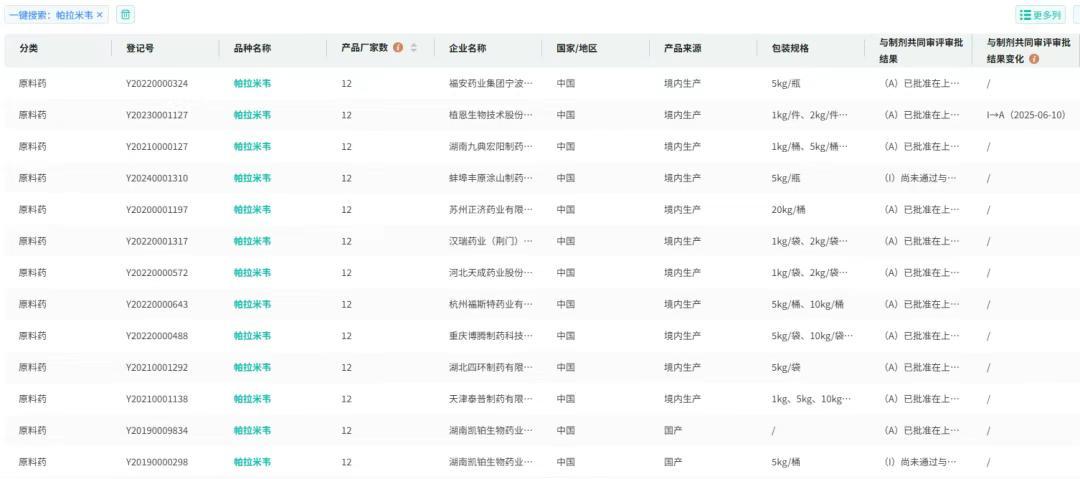 截图来源:摩熵医药CDE原料药、药用辅料和药包材登记信息数据库
截图来源:摩熵医药CDE原料药、药用辅料和药包材登记信息数据库2025年4月7日上海阳光医药采购网公示,取消山西阳和医药帕拉米韦注射液中选资格,将该企业及生产企业山西国润制药列入违规名单,暂停这两家企业2025年4月8日至2026年10月7日参与国家药品集采的申报资格。
 截图来源:上海阳光医药采购网
截图来源:上海阳光医药采购网该企业取消中选资格后,山西、黑龙江、重庆备供厂家分别为广州绿十字、吉林四环、陕西博森生物,中选价分别为14.70元(60ml:0.3g1袋)、5.55元(20ml:0.2g1支)、5.99元。
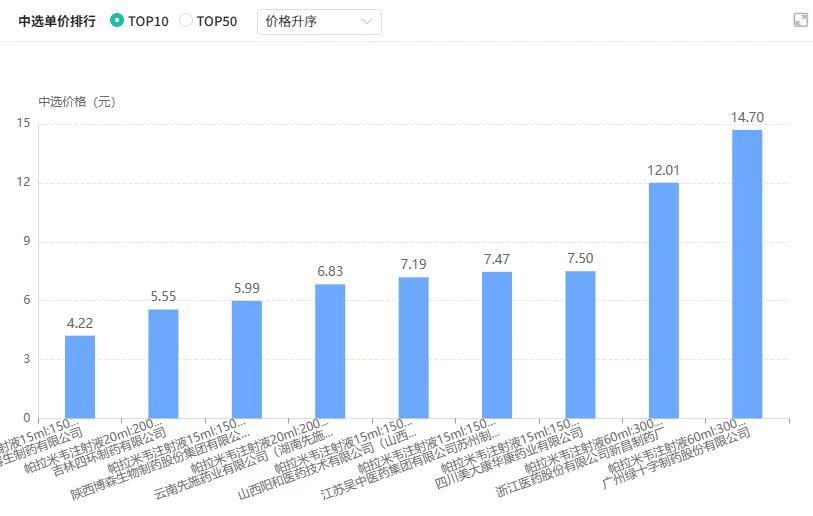 截图来源:摩熵医药药品集中采购数据库
截图来源:摩熵医药药品集中采购数据库作为年销售额超10亿元的抗流感病毒药物,帕拉米韦的市场竞争已趋激烈。从其市场格局的动态演变中不难发现,抗流感药物领域既充满机遇,也面临规范与竞争的双重考验。随着更多企业的深入布局,期待这一领域能在创新与合规的平衡中持续发展,为临床提供更优质、可及的治疗选择。