【新华财经深度报道】新质生产力民企在行动 香雪制药TCR-T细胞治疗新药纳入突破性治疗品种
转自:新华财经
7月30日,来自上市公司广州市香雪制药股份有限公司(股票代码:300147)董事会的一则公告引起投资者广泛关注,公司股价在随后的5个交易日翻倍。
公告称,公司子公司广东香雪精准医疗技术有限公司(以下简称“香雪生命科学”)申报的 TAEST16001 注射液被国家药品监督管理局药品审评中心(以下简称“药审中心”)纳入突破性治疗品种名单。
突破性治疗品种认定政策是中国国家药品监督管理局(NMPA)为加速具有显著临床优势的新药研发和上市进程而推出的重要举措。自2020年实施以来,该政策在促进创新药物快速进入市场、满足临床急需方面发挥了重要作用。从传奇生物“西达基奥仑赛”成为首款中国突破性治疗品种,用于单药治疗复发或难治性多发性骨髓瘤,到现在已有250款药品纳入突破性治疗品种。药审中心认定的突破性治疗药物是选择关注更优秀的临床数据、更差异化的临床靶点、更确定性的疗法,是探寻有价值新药项目的最高切入点,受到了药品研发行业的普遍关注,是目前中国药监体系门槛和含金量最高的资质称谓。
中国国家药品监督管理局 (NMPA) 药品审评中心(CDE)同意香雪生命科学(XLifeSc)的TAEST16001注射液纳入突破性治疗品种名单,标志着该产品作为中国第一个IND获批开展临床试验的TCR-T细胞治疗新药取得重大突破,可加快关键性临床试验和附条件批准上市的进程,有望成为中国第一款上市的TCR-T细胞治疗药物,对中国免疫细胞治疗创新药的发展具有里程碑的意义。
分析人士指出,细胞免疫治疗作为千亿级生物医药产业的重要分支,香雪生命科学搭建了自主开发创新平台,突破TCR-T细胞免疫治疗关键技术,在国内肿瘤细胞免疫治疗领域处于领先地位,达到国际水平,研发的产品可代表广州和中国参与全球竞争,造福患者和社会,成为助力大湾区生物医药产业高质量发展的新标杆。
自主研发的创新革命
TCR-T细胞治疗剑指晚期实体瘤
纳入突破性治疗品种的TAEST16001注射液是香雪生命科学自主研发的一款靶向NY-ESO-1的亲和力增强的TCR-T细胞免疫治疗产品,其首个临床研究适应症是HLA-A*02:01阳性且表达NY-ESO-1抗原的晚期软组织肉瘤患者。该产品是中国首个获得IND批件的TCR-T产品,也是中国唯一进入II期临床的TCR-T产品。
据了解,软组织肉瘤是一组来源于间叶组织的实体恶性肿瘤,恶性程度高常规治疗效果差,其在成人恶性肿瘤中占比约1%,在儿童肿瘤中占比约10%。据统计,14.5%~26.5%的软组织肉瘤患者,在初诊时已发生转移。高级别肉瘤即使经局部手术切除,术后仍有40%~50%的患者会发生远处转移,一旦发生转移,5年生存率不到10%。规范化的诊疗策略对于软组织肉瘤至关重要,但目前临床上仍面临重大挑战。由于不同肉瘤亚型对化疗药物的反应存在显著差异,目前对于局部晚期或转移性软组织肉瘤的一线治疗,主要推荐以蒽环类药物为主的姑息化疗。然而,现有的治疗方案仍存在较大的局限性,临床需求远未得到充分满足。
TAEST16001注射液被纳入突破性治疗品种,有望填补这一临床需求。TAEST16001的I期临床试验结果获得2022年美国临床肿瘤学会(ASCO)年会的认可在肉瘤专场进行口头汇报,在会中首次公开临床试验数据结果显示肿瘤客观缓解率(ORR)达到41.7%,其安全性和有效性的临床研究结果与国外知名药企同靶点产品的临床结果相当,获得了全球参会同行的认可和业界的高度关注。2024年6月,TAEST16001针对晚期软组织肉瘤II期临床试验的阶段性总结数据再次入选ASCO年会,其在II期临床早期数据显示出与之前的I期研究一致的可控的安全性和耐受性。根据RECIST1.1,由独立影像评估委员会(IRC)评估的最佳缓解率为50%(4/8)。由独立影像评估委员会和研究者评估的中位无进展生存期均为5.9个月。TAEST16001对经标准全身系统治疗失败而缺乏有效治疗选择的晚期软组织肉瘤的人群,观察到显著临床意义的疗效和可控的安全性。
截至目前,全球范围内共有4款TCR-T产品在治疗软组织瘤的临床中取得进展,其中TAEST16001是唯一的中国自主研发TCR-T细胞治疗产品。其他三款均为海外企业研发,尚未在国内开展临床试验。TAEST16001被纳入突破性治疗药物不仅为软组织肉瘤患者提供了新的治疗选择,也标志着中国自主研发的TCR-T细胞治疗产品在国际竞争中迈出了重要一步。
晚期实体瘤是临床亟需解决的医学需求,近年来免疫细胞治疗的研究进展为攻克实体瘤带来了新的希望。2024年2月,全球首款肿瘤浸润淋巴细胞(TIL)疗法Amtagvi获得美国食品药品监督管理局(FDA)的批准,用于治疗晚期黑色素瘤,这无疑是细胞疗法在实体瘤治疗领域取得的重大进展。除了TIL疗法,TCR-T 是另一备受行业看好的实体瘤细胞疗法,作为一种基因工程标准化生产的细胞疗法,TCR-T具有成为通用型产品的潜力,这不仅有助于降低生产成本,也极大提高了治疗的普及性和可及性。
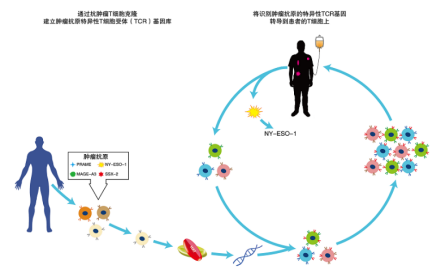
当前,免疫细胞治疗市场上的产品以CAR-T细胞疗法为主导,其应用主要集中在血液瘤的治疗上。然而,随着每年新发肿瘤患者数量的不断攀升,其中超过90%的患者面临的是实体瘤的挑战。对于晚期实体瘤患者来说,现有的治疗选择相对有限。不过随着细胞疗法的持续发力,特别是TCR-T细胞疗法在实体瘤治疗领域取得了突破性的发展,为患者带来了新的希望和机遇。
据统计,中国免疫细胞治疗市场正迅速扩张,预计从2021年的13亿元增长至2030年的584亿元,年均增长率达到53%。在这一增长中,CAR-T细胞疗法市场预计将从2亿-3亿元增长至287亿元,而包括TCR-T在内的其他细胞治疗市场将从10亿元增长至297亿元。
香雪生命科学作为TCR-T细胞免疫治疗头部企业,拥有全球最多的TCR-T在研新药品种,靶点丰富涉及包括CT抗原,新生抗原,病毒抗原等几乎所有与肿瘤相关的特异性抗原,涵盖A0201,A1101及A2402等多个以中国人群居多的HLA基因型,适应症覆盖多种临床难治的实体瘤。适应症覆盖使得TCR-T疗法在肿瘤治疗领域具有巨大的应用潜力和实际价值,预计将承载超过100亿美元的产业规模。
瞄准产业前沿
医药新质生产力实践探索
国家层面对创新药物发展的全链条支持已经全面铺开,预示着国产创新药物即将迎来快速发展的新阶段。2024年7月,国务院常务会议审议通过了具有里程碑意义的《全链条支持创新药发展实施方案》。该方案的核心目标是通过政策的有力引导和全方位支持,全面加速创新药物的研发进程、优化审批流程、扩大临床应用,并完善医保支付体系等关键环节。
《全链条支持创新药发展实施方案》的发布,不仅彰显了中国政府对医药产业创新的高度重视,更是体现了国家致力于满足人民群众的健康需求、提升国内医药产业的创新实力以及增强其在国际舞台上的竞争力的坚定决心。这一系列举措将为国产创新药物的发展注入强劲动力,助力其在新的发展阶段实现“起飞”。
在这一政策的推动下,国产创新药物的国际化步伐也正加速推进。近日,细胞疗法领域的领军企业传奇生物收到并购邀约的消息,在生物医药领域引起了轩然大波。传奇生物核心产品CAR-T(西达基奥仑赛)已在美国及欧洲市场取得了显著的成绩,展现出巨大的市场潜力和国际竞争力。
业内猜测,如果以30%-50%的溢价来算,此次交易收购价或将在130亿-150亿美元之间,将创造中国biotech公司被收购的新纪录。这起并购邀约不仅是对传奇生物科研成就和市场影响力的肯定,也象征着中国创新药物在全球医药市场中的竞争力。在国家政策的有力支持和全球市场需求的推动下,国产创新药物正稳健地迈向国际舞台。
事实上,随着国家对生物医药产业的重视和支持力度不断加大,国产创新药的发展迎来了前所未有的机遇。
《中共中央关于进一步全面深化改革、推进中国式现代化的决定》的发布为生物医药产业的高质量发展指明了方向,提出健全因地制宜发展新质生产力的体制机制。加强关键共性技术、前沿引领技术、现代工程技术、颠覆性技术创新,加强新领域新赛道制度供给,建立未来产业投入增长机制,完善推动新一代信息技术、人工智能、航空航天、新能源、新材料、高端装备、生物医药、量子科技等战略性产业发展政策和治理体系,引导新兴产业健康有序发展。
香雪生命科学作为广州本土的生物医药企业,在因地制宜发展医药新质生产力的实践探索中,积极响应《广州促进生物医药产业高质量发展的若干政策措施》,通过一系列创新举措,致力于推动医药产业的创新和高质量发展。
香雪生命科学
聚焦“产研学”十年磨一剑
作为TCR-T细胞免疫治疗头部企业,香雪生命科学以“解决人类健康难点,树立肿瘤治疗标杆”为愿景,以“聚焦TCR,赋能T细胞,攻克实体瘤”为使命。拥有高技术壁垒的TCR-T核心研发技术平台、高效筛选候选药物的体系和全球第一条全自动的细胞制备平台和细胞产品质控体系;针对中国人种基因型已储备20多个临床价值极高的实体瘤管线。立足粤港澳大湾区,辐射广东和全国,影响全球,为国内外患者提供疾病个体化精准的诊断和TCR-T为主的免疫细胞治疗全面解决方案,为肿瘤治疗带来新突破,成为助力区域健康产业发展新引擎。
 (香雪生命科学实验室)
(香雪生命科学实验室)基于广州及区域生物医药产业优势基础,香雪生命科学积极推动上下游产业链的联动,形成产业集群效应。通过与高校、科研机构的紧密合作,实现“产研学”一体化发展,加速科研成果的转化和应用,提升区域生物医药产业的整体竞争力。进一步以创新驱动带动免疫细胞治疗产业发展,助力区域成为生物医药发展核心引擎 ,助力广州打造TCR-T细胞治疗策源地。
香雪制药董事长王永辉表示:“我们从2012年开始投入香雪TCR-T项目,十年磨一剑,如今终于获得一定成果,企业家要有梦想和情怀,坚持创新和投入。”众所周知,创新药物的研发是一场漫长而充满挑战的旅程。据介绍,香雪生命科学TCR-T细胞疗法项目依托母公司香雪制药上市后募集的资金,接连引进来自英国、德国、美国等发达国家的20多位“海归”科学家,组成强大的科研团队,成立香雪生命科学中心,专注研发生物医药领域的前沿技术。十年磨一剑,香雪制药的坚持和创新精神终于开花结果。TCR-T细胞疗法领域取得了突破性进展,是企业家梦想与情怀的体现,也是对持续创新和投入的最好回报。
 (香雪生命科学研究人员进行实验)
(香雪生命科学研究人员进行实验)公司公告称,以广州中山大学肿瘤防治中心和北京大学肿瘤医院作为牵头单位开展临床试验,目前已完成 I 期临床试验和 II 期临床试验第一阶段的研究工作,对经标准全身系统治疗失败而缺乏有效治疗选择的晚期软组织肉瘤的人群,观察到显著临床意义的疗效和可控的安全性。
公司认为,TAEST16001 注射液作为具有突破性的疗法药物,将在药审中心的指导下加快开展关键性临床试验和附条件批准上市的步伐,力争成为中国第一个获批上市的 TCR-T 细胞治疗创新药物。如果产品能够获批上市,确立公司在 TCR-T 免疫细胞治疗的领先地位,有利于增强公司的核心竞争力。
香雪生命科学通过医药新质生产力实践探索,体现了中国生物医药企业在新质生产力发展中的积极作为。通过创新驱动、区域联动、全方位支持和成果转化,香雪生命科学正助力广州乃至全国的生物医药产业实现高质量发展,占据全国乃至全球的科技创新发展核心战略地位。这不仅是企业自身的发展需求,更是对国家战略的积极响应和贡献。
免责