2023ESMO开幕︱恒瑞医药36项抗肿瘤创新药研究亮相,向世界彰显中国医药创新力
北京时间10月20日,2023年欧洲肿瘤内科学会(ESMO)大会在西班牙马德里正式开幕。作为全球最具影响力的肿瘤学会议之一,世界顶尖专家齐聚于此,探讨、分享当前国际最前沿的肿瘤学科研成果和肿瘤治疗技术。
本届大会,作为中国医药创新代表性企业的恒瑞医药共有13款抗肿瘤创新药的36项研究成果入围【1】,其中2项入选优选口头(Proffered Paper)报告,6项研究入选简短口头(Mini Oral)报告,28项研究接收为壁报,覆盖消化道肿瘤、乳腺癌、宫颈癌、胰腺癌、肺癌、黑色素瘤、肉瘤、胆管癌等十余个领域。
13款抗肿瘤创新药包括6款已上市产品:注射用卡瑞利珠单抗(艾瑞卡)、甲磺酸阿帕替尼片(艾坦)、马来酸吡咯替尼片(艾瑞妮)、阿得贝利单抗注射液(艾瑞利)、氟唑帕利胶囊(艾瑞颐)、瑞维鲁胺片(艾瑞恩),以及7款未上市产品:多靶点受体酪氨酸激酶抑制剂法米替尼、KRAS G12D抑制剂HRS-4642、抗PD-L1/TGF-βRII双抗SHR-1701、组蛋白甲基转移酶EZH2抑制剂SHR2554、HER2抗体偶联药物(ADC)SHR-A1811、HER3抗体偶联药物SHR-A2009、新型选择性雌激素受体共价拮抗剂(SERCA)HRS8807等。
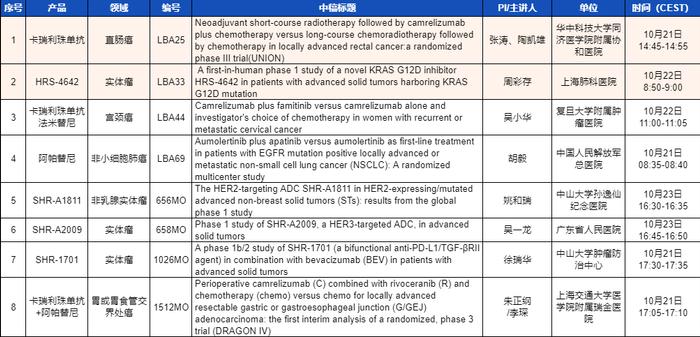
2023ESMO年会,恒瑞医药产品相关研究2项入选优选口头报告,6项入选简短口头报告
消化系统肿瘤领域:
卡瑞利珠单抗直肠癌研究入选优选口头报告
在消化系统肿瘤领域,恒瑞创新产品相关研究共入选1项优选口头报告、1项简短口头报告和11项壁报展示。除了经典的明星药物卡瑞利珠单抗和阿帕替尼,SHR-A1811、SHR-1701等未上市创新产品也有相应研究入选。此外,阿得贝利单抗、氟唑帕利等已上市药物也在积极探索新的适应症,本次ESMO大会分别有肝内胆管癌和胰腺癌相关研究入选。这些新老药物前沿研究的不断出现,有望为消化系统肿瘤患者带来新的福音!
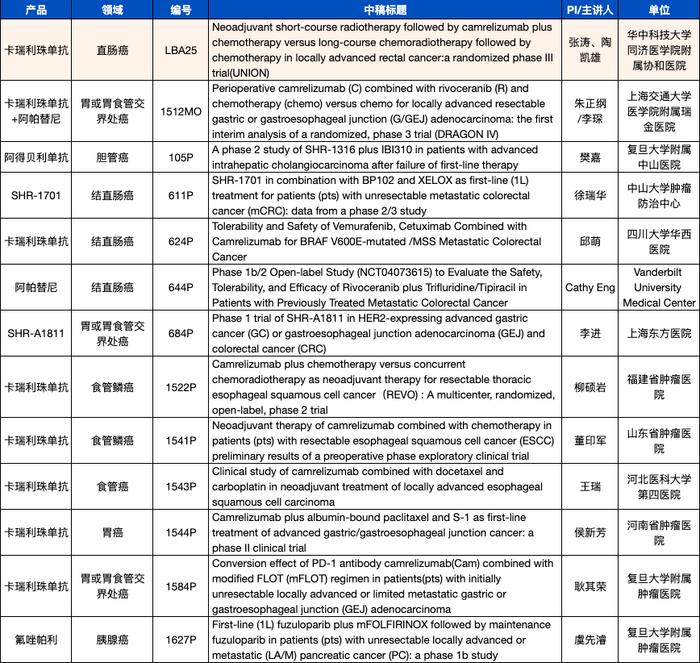
由华中科技大学同济医学院附属协和医院张涛教授、陶凯雄教授担任主要研究者的“新辅助短程放疗序贯卡瑞利珠单抗联合化疗对比长程放化疗序贯化疗治疗局部晚期直肠癌随机对照Ⅲ期试验(UNION)”被接收为LBA优选口头报告【2】。UNION研究共纳入231例患者,随机分配到卡瑞利珠单抗联合化疗(CAM+CAPOX)组和化疗(CAPOX)组。CAM+CAPOX组39.8%的患者达到pCR,而CAPOX组为15.3%,CAM+CAPOX组的pCR率显著优于CAPOX组,差异具有统计学意义(OR3.7 [95% CI:2.0-6.9], p研究结果表明,与长程放化疗序贯化疗相比,围手术期短程放疗序贯卡瑞利珠单抗联合化疗显示出更高的pCR率和可接受的安全性,为卡瑞利珠单抗在直肠癌领域的治疗再添力证!
以上海交通大学医学院附属瑞金医院朱正纲教授担任主要研究者的“卡瑞利珠单抗联合阿帕替尼和化疗对比化疗治疗局部进展期胃癌”随机对照Ⅲ期试验(DRAGON-IV/AHEAD-G208)成功入选简短口头报告【3】。研究结果显示,意向治疗人群(ITT)中,阿帕替尼250mg+卡瑞利珠单抗200mg+SOX方案新辅助治疗后接受手术患者的术后病理完全缓解(pCR)率高达18.3%,显著高于SOX方案(奥沙利铂+替吉奥)化疗组的5.0%。这一结果不仅有力地证实了靶免化联合疗法机制切实可行,还丰富了广大胃癌患者围术期治疗选择,为其长期生存获益带来全新希望。
乳腺癌领域:
吡咯替尼6项研究入选
在乳腺癌领域,吡咯替尼、阿帕替尼、卡瑞利珠单抗、法米替尼,或产品间联合或联合化疗,共有9项研究入选,其中吡咯替尼占据6项,较为全面地展示了这款中国首个自主研发抗HER2靶向药在乳腺癌治疗中的显著特点和潜力。此外,恒瑞医药自主研发的新型选择性雌激素受体共价拮抗剂(SERCA)HRS8807治疗ER+/HER2-局部晚期或转移性乳腺癌的Ⅰ期研究也成功入选,有望为此类患者带来更多用药新选择。
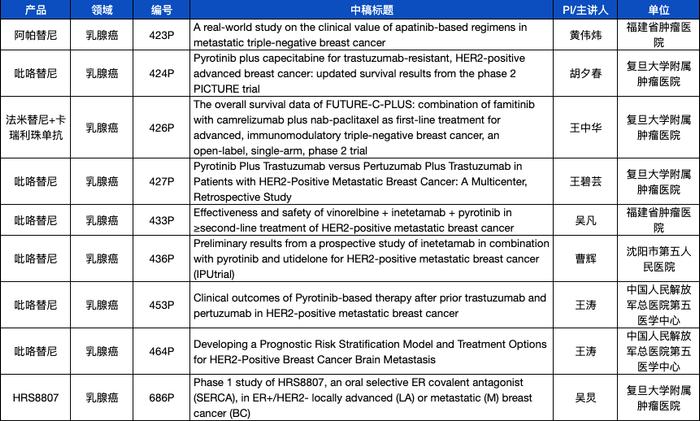
宫颈癌领域:
卡瑞利珠单抗联合法米替尼齐发力

在宫颈癌领域,由复旦大学附属肿瘤医院吴小华教授团队开展的“卡瑞利珠单抗联合法米替尼对比卡瑞利珠单抗单药或研究者选择化疗治疗复发转移性宫颈癌”研究成功入选LBA简短口头报告【4】。该研究共纳入194例患者,随机分配至A组(卡瑞利珠单抗联合法米替尼)、B组(卡瑞利珠单抗单药)、C组(研究者选择化疗)。主要研究终点为BICR评估的A组对比B组的客观缓解率(ORR),结果显示A组的ORR为41.0%,B组为24.1%。经研究者评估,A组ORR为42.9%,疾病控制率(DCR)74.3%,无进展生存期(PFS)为8.1个月;B组ORR为22.2%,DCR53.7%,PFS为4.1个月;C组ORR为14.3%,DCR42.9%,PFS为2.9个月。此项研究表明,卡瑞利珠单抗联合法米替尼用于复发转移性宫颈癌在客观缓解率及无进展生存期等方面显示获益,且安全性良好,有望成为广大宫颈癌患者新的曙光。
肺癌领域:
卡瑞利珠单抗、阿帕替尼再探索
在肺癌领域,恒瑞创新药卡瑞利珠单抗、阿帕替尼共有3项研究入选。

其中,阿帕替尼联合其他公司创新药的一项研究入选了LBA简短口头报告,即“阿美替尼联合阿帕替尼对比阿美替尼单药一线治疗EGFR突变的局晚或转移性非小细胞肺癌(NSCLC): 一项随机多中心临床研究”【5】,由中国人民解放军总医院胡毅教授担任主要研究者。该研究共纳入104例患者,其中98例纳入疗效分析集。截至2023年9月12日,阿美替尼联合阿帕替尼组和阿美替尼组的总体ORR分别为72.9%和64%,DCR分别为100%和94%。在EGFR敏感突变亚组中,阿美替尼联合阿帕替尼组和阿美替尼组的ORR分别为75%和68%。在脑转移和肝转移亚组中,阿美替尼联合阿帕替尼组和阿美替尼组的ORR分别为100%和60%,60%和33%,颅内ORR(iORR)分别为82%和63%。阿美替尼联合阿帕替尼组有PFS获益趋势。该研究结果表明,阿美替尼联合阿帕替尼为EGFR突变NSCLC一线治疗,提供了一种更有效且安全性良好的治疗选择。
实体瘤:
多项上市前研究入选口头报告
彰显恒瑞强大研发实力

本次ESMO大会,恒瑞多款上市前创新药物HRS-4642、SHR-A1811、SHR-A2009、SHR-1701治疗实体瘤相关研究入选口头报告,展现了恒瑞医药强大的自主研发能力。
由上海肺科医院周彩存教授担任主要研究者的“新型KRAS G12D抑制剂HRS-4642治疗KRAS G12D突变晚期实体瘤患者的首次人体I期研究”成功入选LBA优选口头报告【6】。该研究共纳入18例患者,未观察到剂量限制性毒性(DLTs),未达到最大耐受剂量(MTD),不良反应发生率无剂量依赖趋势。13例患者至少进行了一次基线后评估,1例NSCLC患者接受200mg治疗有部分缓解。11例(61.1%)疾病稳定,6例(33.3%)靶病灶缩小,包括肺癌和结直肠癌。HRS-4642治疗KRAS G12D突变的晚期实体肿瘤显示出安全可耐受和初步抗肿瘤活性。HRS-4642剂量爬坡正在进行中,预计不久将进入剂量扩展阶段。
由中山大学孙逸仙纪念医院姚和瑞教授担任主要研究者的“靶向HER2-ADC SHR-A1811治疗HER2表达/突变的晚期非乳腺的实体瘤(STs):来自全球1期研究的结果”成功入选简短口头报告【7】。该研究共纳入98例非乳腺晚期实体瘤患者,其中85例患者可评估,ORR为45.9%(39/85;95%CI:35.0-57.0);DCR为88.2%(75/85;95%CI:79.4-94.2);中位TTR为1.4个月(范围0.7–5.8)。HER2、IHC3+患者ORR为54.1%(20/37),IHC2+患者为41.7%(10/24),IHC1+患者为50.0%(7/14)。对于不同肿瘤类型,胆道恶性肿瘤患者的ORR为60.0%(9/15),尿路上皮癌患者为59.1%(13/22),胃或胃食管连接部癌(GC/GEJC)患者为50.0%(6/12),结直肠患者为36.4%(4/11)。该研究结果显示,SHR-A1811对HER2表达/突变的晚期非乳腺实体瘤具有良好的抗肿瘤活性和可接受的安全性。
由广东省人民医院吴一龙教授为主要研究者的“HER3靶向ADC药物SHR-A2009治疗晚期实体瘤的I期研究”成功入选简短口头报告【8】。该研究共纳入42例患者,在可评估患者中,所有患者(全瘤种)ORR为25.0%(9/36;95% CI:12.1- 42.2),NSCLC患者ORR为30.0%(9/30;95% CI:14.7-49.4);两组患者的中位缓解持续时间(DoR)均为7.0个月(范围2.8-8.5)。所有患者(全瘤种)的6个月PFS率为46.4%(95% CI:27.0-63.8),NSCLC患者的6个月的PFS率为49.8%(95% CI:28.8-67.8)。该研究结果表明,SHR-A2009在经治晚期实体瘤患者中显示出可控的安全性和令人鼓舞的抗肿瘤活性。该研究正在进行中,探索SHR-A2009的更高耐受剂量和可治疗的瘤种类型(NSCLC和其他实体肿瘤)。
由中山大学肿瘤防治中心徐瑞华教授担任主要研究者的“SHR-1701联合贝伐珠单抗(BEV)治疗晚期实体瘤患者的1b/2期研究”成功入选简短口头报告【9】。该研究共纳入67例晚期实体瘤患者,包括19名HER2 阴性、PD-L1阳性(CPS ≥1)的初治胃或胃食管连接部癌(GC/GEJC)患者、27名接受过治疗的GC/GEJC患者和10名接受过治疗的非鳞状非小细胞肺癌(nsqNSCLC)患者,其ORR分别为21.1%、33.3%、10.0%。在PD-L1 CPS ≥5的经治GC/GEJC患者中,ORR达77.8%,中位PFS达10.3个月。经治nsqNSCLC患者的中位PFS为6.2个月。该研究表明,SHR-1701联合BEV在晚期GC/GEJC和nsqNSCLC患者中显示出令人鼓舞的抗肿瘤活性和良好的安全性,为后续GC/GEJC和nsqNSCLC的相关研究开辟了一条崭新道路!
其他肿瘤领域:
瑞维鲁胺等5款创新药
在多瘤种全面发力
此外,在前列腺癌、黑色素瘤、肉瘤、下咽癌、肺外神经内分泌癌等多个领域,卡瑞利珠单抗、阿帕替尼、瑞维鲁胺、SHR-1701、SHR-2554等产品相关研究一共入选了6项壁报展示,彰显了恒瑞医药强大的综合实力。

本届ESMO大会,恒瑞医药多项重磅创新研究再次闪耀国际学术舞台,既是国际学术界对恒瑞医药抗肿瘤领域自主研发创新实力的一大认可,更彰显了我国医药创新在全球的重要力量和责任担当。
作为创新型国际化制药企业,恒瑞医药多年来针对中国高发肿瘤领域持续推进创新研发。目前,公司已在中国获批上市自研1类创新药13款、2类改良型新药1款、引进创新药2款,其中肿瘤创新药达9款。未来,恒瑞医药将继续坚持“以患者为中心”的理念,重创新,强研发,力争研制出更多更好的新药,服务健康中国,惠及全球患者。
参考资料:
1. https://cslide.ctimeetingtech.com/esmo2023
2. Neoadjuvant short-course radiotherapy followed bycamrelizumab plus chemotherapy versus long-course chemoradiotherapy followed bychemotherapy in locally advanced rectal cancer:a randomized phase IIItrial(UNION). ESMO 2023:LBA25
3. Perioperative camrelizumab (C) combined with rivoceranib(R) and chemotherapy (chemo) versus chemo for locally advanced resectablegastric or gastroesophageal junction (G/GEJ) adenocarcinoma: the first interimanalysis of a randomized, phase 3 trial (DRAGON IV).ESMO 2023:1512 MO
4. Camrelizumab plus famitinib versus camrelizumab alone andinvestigator's choice of chemotherapy in women with recurrent or metastaticcervical cancer. ESMO 2023:LBA 44
5. Aumolertinib plus apatinib versus aumolertinib asfirst-line treatment in patients with EGFR mutation positive locally advancedor metastatic non-small cell lung cancer (NSCLC): A randomized multicenterstudy.ESMO 2023:LBA 69
6. A first-in-humanphase 1 study of a novel KRAS G12D inhibitor HRS-4642 in patients with advancedsolid tumors harboring KRAS G12D mutation.ESMO 2023:LBA 33
7. The HER2-targeting ADC SHR-A1811 inHER2-expressing/mutated advanced non-breast solid tumors (STs): results fromthe global phase 1 study. ESMO 2023:656MO
8. Phase 1 study of SHR-A2009, a HER3-targeted ADC, inadvanced solid tumors.ESMO 2023:658MO
9. A phase 1b/2 study of SHR-1701 (a bifunctionalanti-PD-L1/TGF-βRII agent) in combination with bevacizumab (BEV) in patientswith advanced solid tumors.ESMO 2023:1026 MO.