HPV疫苗研发进程或提速,万泰生物九价疫苗率先上市几率多大?
尽管万泰生物在二价HPV疫苗上抢得先机,但在九价HPV疫苗的研发上,公司面临的竞争更为激烈

《投资时报》研究员罗艺
7月11日,国家药监局发布通告,正式公布《人乳头瘤病毒疫苗临床试验技术指导原则(试行)》(下称《指导原则》)。该《指导原则》自公布之日起施行。
作为全球的爆款疫苗,拥有巨大市场缺口的人乳头瘤病毒疫苗(下称HPV疫苗》,一直有很高的市场关注度,尤其是“一针难求”的九价疫苗。拥有国内首个获批上市二价HPV疫苗的万泰生物(603392.SH)),自然也成为新一轮HPV浪潮中被市场重点关注的对象。不久前,万泰生物对外透露,公司九价HPV疫苗Ⅲ期临床试验正按方案进行访视并进入关键阶段。
按照《指导原则》,此前有HPV疫苗研发平台基础,即第一代疫苗的企业,在开发迭代疫苗时可在一定程度上加速临床试验。目前,国内推出二价HPV疫苗的企业包括万泰生物和沃森生物,市场认为,它们或是这一政策的首批受益者。
同时,《投资时报》研究员注意到,除万泰生物外,国内还有沃森生物、上海博唯、康乐卫士及瑞科生物旗下的九价HPV疫苗进入临床三期阶段。有机构预测,国产九价HPV疫苗最早或于2025年左右投入市场。
信息显示,万泰生物二价HPV疫苗于2019年12月30日获批上市,并于2020年5月正式投入市场。自2020年以来,该疫苗产品一直是促使万泰生物业绩飙升的主要动力。2020年—2022年,该公司营收分别为23.54亿元、57.50亿元和111.85亿元,分别同比增长98.88%、144.25%和94.51%。
万泰生物的九价HPV疫苗能否率先上市?面对更多的竞争者,公司能持续保持高利润和高增长吗?针对上述问题,《投资时报》研究员电邮沟通提纲至该公司相关部门,截至发稿尚未收到回复。
万泰生物2022年主要经营数据
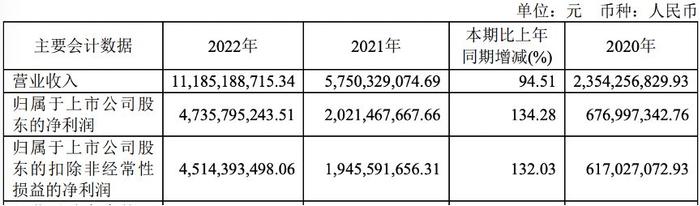
数据来源:公司年报
HPV疫苗研发进程有望提速
国家药监局发布的《指导原则》之所以引发市场广泛关注,在于其有可能加快HPV疫苗的上市步伐。《指导原则》指出,根据有无HPV疫苗研发平台基础,可大致分为第一代疫苗和迭代疫苗。第一代疫苗为企业首次研发的HPV疫苗,一般情况下覆盖的HPV型别有限;迭代疫苗则是疫苗企业基于第一代疫苗研发平台开发的疫苗。
据了解,HPV疫苗研发过程中的保护效力数据,一直以来以宫颈鳞状细胞癌(CIN2+)和腺癌的癌前病变或宫颈癌等组织病理学为终点。但《指导原则》指出,若上一代疫苗采用公认的组织病理学终点,符合上市要求,且试验疫苗经药学评估确属迭代疫苗,则可按病毒学终点12个月高危型持续感染(PI12)申报上市,以缩短获批上市的时间。
《指导原则》指出,一般情况下,PI12定义为在相隔5—7个月采集的人体相关成分中,连续3次及以上经PCR发现同一HPV型别核酸阳性。这表明,迭代疫苗最快可在12个月的临床试验后就申报上市。同时,《指导原则》要求HPV疫苗上市后的受试者随访,应至少持续至全程免疫后72个月,鼓励更长期的有效性和安全性观察。
对比默沙东四价HPV疫苗在国内上市时的临床试验周期可以看到,2009年2月,默沙东四价HPV疫苗在国内开始III期临床试验。当时,默沙东预期试验时间为3年,但最终于2017年5月才获批上市。
而试验未能如期结束的一个重要原因,即当时为确保安全,相关疫苗临床试验以癌变指征作为终点。试验过程中需要以安慰剂做对照组,但通常情况下,对照组中人体感染HPV后进展为子宫颈癌,一般需要10年—20年,这无疑拉长了试验的周期。
《指导原则》一出,市场认为首批红利享受者当属已有二价疫苗上市的万泰生物和沃森生物,这两家企业的九价HPV疫苗均处在III期临床试验中。
万泰生物在投资者互动平台上表示,公司九价HPV疫苗III期临床正按方案进行访视并进入关键阶段。此外,万泰生物还透露,目前公司暂无将九价HPV疫苗生产线用于二价HPV疫苗生产的计划。
市场竞争渐趋激烈
《投资时报》研究员注意到,在国内已经上市的HPV疫苗中,按照对抗几种HPV病毒来分类,可分为二价、四价、九价三种疫苗,价次越高,开发难度越大。其中,九价疫苗的获批厂商目前只有默沙东。
观察默沙东四价和九价HPV疫苗的中国代理商智飞生物的财报,可以发现HPV疫苗在中国市场的巨大商业价值。2012年和2018年,智飞生物先后拿下默沙东四价与九价HPV疫苗在中国大陆市场的进口、经销和推广权。2022年,智飞生物实现营收382.64亿元,其中,代理产品收入占九成,这其中批签发量最大的为默沙东九价HPV疫苗“佳达修9”。
智飞生物年报显示,2022年,九价HPV疫苗批签发1547.72万支,增长率为51.65%,四价HPV疫苗批签发1402.84万支。
万泰生物的HPV疫苗项目最早立项于2003年。农夫山泉创始人钟睒睒在2001年以1710万元买下当时经营不善的万泰生物95%股权后,与厦门大学相关研究机构合作,经过戊肝疫苗的最初尝试之后,开始涉足HPV疫苗领域。
彼时,默沙东的全球首个四价HPV疫苗正处在最后临床试验阶段。2006年,默沙东四价HPV疫苗“佳达修”在美国上市;2007年,英国葛兰史素克研发并上市全球第一款二价HPV疫苗。
据公开信息显示,万泰生物二价HPV疫苗于2019年12月30日获批上市,并于2020年5月正式投入市场实现销售收入。如从最早立项的2003年算起,开发周期长达17年。但自上市后,HPV疫苗迅速超过万泰生物体外检测业务,成为公司业绩增长的最大贡献者。
那么,《指导原则》的出台,能否促使万泰生物成为率先上市国产九价HPV疫苗产品的企业?不少市场人士认为,尽管万泰生物在二价HPV疫苗上抢得先机,但在九价HPV疫苗的研发上,公司面临的竞争更为激烈。据不完全统计,目前,除万泰生物外,国内还有沃森生物、上海博唯、康乐卫士及瑞科生物旗下的九价HPV疫苗进入临床三期阶段。
二价HPV疫苗带来业绩高增
《投资时报》研究员注意到,在2020年二价HPV疫苗上市之前,万泰生物营收主要来源于诊断试剂。财报数据显示,2017年—2019年,该公司诊断试剂(自有)销售收入分别为7.55亿元、7.86亿元、9.65亿元,占总营收比为81.73%、83.36%、83.77%,同期,戊肝疫苗销售占比仅为0.35%、0.87%和1.3%。
2020年5月,万泰生物的二价HPV疫苗正式投入市场。相较于已上市的葛兰史素克的二价HPV疫苗和默沙东的四价和九价HPV疫苗,万泰生物的二价HPV疫苗具有接种程序少且价格更低的优势。
二价HPV上市当年,万泰生物营收在上年基础上增加11.71亿元,达23.54亿元。其中,二价HPV疫苗获得营收6.93亿元。2021年,公司业绩继续大涨,营收同比增144.25%至57.50亿元,归母净利润同比增198.59%至20.21亿元。2022年,万泰生物营收突破百亿,达111.85亿元。
据2022年报显示,万泰生物二价HPV疫苗在药品集中招标采购中,中标价格为329元/瓶—344元/瓶,医疗机构的合计实际采购量为2569.10万瓶,万泰生物从中获得营收84.52亿元至88.38亿元,占总营收比超七成。
但万泰生物二价HPV疫苗也将不再一家独大,2022年它迎来了新的竞争对手。信息显示,2022年3月,沃森生物旗下的二价HPV疫苗获批上市,成为国内第二家能够上市生产销售二价HPV疫苗的企业。
根据沃森生物公布的信息,去年9月,公司拿下福建省疾控中心HPV疫苗采购项目价值1.42亿元大单。据采购信息显示,该项目购买量为58万支,按此计算,中标价格为245元/支,与万泰生物的价格相比低出不少。在这一过程中,万泰生物能否维持稳定的市场份额和高利润还未可知。