新华健康丨博瑞医药披露自研重磅药物“头对头”试验数据 多项关键指标优于阳性对照药
转自:衡水日报
近日,博瑞医药(688166.SH)公布了一项在中国2型糖尿病患者中进行的II期临床试验结果,阳性对照药为司美格鲁肽注射液1.0 mg。试验结果显示,BGM0504注射液治疗2型糖尿病的Ⅱ期临床试验多项指标优于阳性对照药,初步结果达到试验预期目标。
值得注意的是,此次BGM0504的II期临床试验采用了“头对头”司美格鲁肽的设计。本次试验共纳入了64例中国2型糖尿病受试者。试验结果显示,在2型糖尿病患者中,BGM0504在降糖效果明显优于司美格鲁肽。BGM0504临床试验效果也超过了替尔泊肽文献数据公布的降糖效果。同时,在中国人群中,对比司美格鲁肽,BGM0504也展现了较强优势。不过,最终的降糖疗效还需要后续大样本量上中国成人2型糖尿病受试者Ⅲ期确证性临床研究来进一步确认。
降糖试验“头对头”
此次初步试验数据公布后,BGM0504注射液的II期临床研究顾问北京大学人民医院纪立农教授表示,期待BGM0504注射液可以为中国2型糖尿病患者的疾病管理提供更多的药物治疗选择。
“头对头”(Head-to-Head)试验,是指在临床试验中将两种或多种已经在临床上使用的治疗药物或治疗方法进行直接比较,而不是使用安慰剂作为对照。这种试验设计的目的是为了评估和比较这些药物或治疗方法在有效性和安全性方面的差异。
BGM0504注射液是博瑞医药(688166.SH)自主研发的GLP-1(胰高血糖素样肽1)和GIP(葡萄糖依赖性促胰岛素多肽)受体双重激动剂,可激动GIP和GLP-1下游通路,产生控制血糖、减重和治疗非酒精性脂肪性肝炎(NASH)等生物学效应。
根据公告,BGM0504本项研究共纳入了64例中国2型糖尿病受试者,其基线平均糖化血红蛋白(HbA1c)8.0%,平均体重76kg,各组基线特征基本均衡。BGM0504注射液目标剂量为5mg、10mg、15mg。
具体来看,BGM0504注射液各剂量组和司美格鲁肽注射液HbA1c较基线平均降幅(扣除安慰剂)分别为1.99%、2.21%、2.76%和1.71%。其中BGM0504注射液15mg组与司美格鲁肽注射液疗效差异为1.05%。
BGM0504注射液各剂量组和司美格鲁肽注射液控糖达标率方面(给药治疗后HbA1c<7.0%的受试者比例)分别为76.9%、81.8%、91.7%和75%。其中中高剂量组中分别有27.3%和50%的受试者达到了糖化正常水平(HbA1c<5.7%),远高于司美格鲁肽注射液组的12.5%。
需要强调的是,1mg是司美格鲁肽在降糖适应症上允许注射的最大剂量。而BGM0504的最小剂量5mg的降糖效果在不同给药周期均已经超过了司美格鲁肽最大剂量的降糖效果。
BGM0504注射液在HbA1c/体重复合达标率方面也显现出明显优势,其中中高剂量组分别有27.3%和41.7%的受试者在使用BGM0504注射液后可以达到HbA1c<6.5%且体重同时相对基线降低≥10%的水平,而司美格鲁肽注射液组仅为6.3%。
HbA1c<7.0%、HbA1c<6.5%、HbA1c<5.7%分别意味着什么呢?
我国2023年发布的《国家标准化代谢性疾病管理中心(MMC)代谢病管理指南(第二版)》指出:对多数非妊娠成人患者,HbA1c<7%可以减少糖尿病微血管并发症;对病程较短、预期寿命较长,且未合并心血管疾病的2型糖尿病患者,在无低血糖或其他药物不良反应的情况下,建议更为严格的HbA1c<6.5%;HbA1c处于5.7%~6.4%之间的人群是发展为糖尿病的高危人群,建议早期进行筛查、随访及干预,控制HbA1c<5.7%可延缓甚至避免其进展为糖尿病。
这意味着按照BGM0504II期临床试验的降糖数据,2型糖尿病患者如果使用15mg高剂量组BGM0504注射液,91.7%的患者可以减少糖尿病微血管并发症,41.7%的患者可以同时满足HbA1c/体重复合达标率,50%的早期高危人群可以逆转为非糖尿病患者。对于广大2型糖尿病患者而言,BGM0504无疑是带来了更大的希望。
起效快也是BGM0504的一大特点。数据显示,当目标剂量给药第4周时,BGM0504注射液5mg组、10mg组、15mg组和司美格鲁肽注射液HbA1c较基线平均降幅(扣除安慰剂)分别为1.32%、1.48%、2.16%和1.03%。
此外,在体重方面,BGM0504各剂量组与基线相比均有不同程度的降低,其中中高剂量组体重下降分别可达4.8kg和7.9kg,司美格鲁肽注射液组下降仅为2.7kg。
一般认为,糖尿病患者减重效果明显不如健康的肥胖患者。且两者的平均体重也有较大差异,后者体重明显大于前者,而BGM0504二期降糖试验的受试者平均体重为76kg。有分析人士指出,目前已有的GLP-1的降糖临床的减重数据均比同品种单独减重临床数据要差,因此不能直接将糖尿病临床数据中的体重数据与单独减重临床混淆,司美格鲁肽、替尔泊肽均是如此。Tirzepatide的SURPASS-1研究中,治疗周期40周后,10mg组体重下降7.0kg 、15mg组体重下降7.8kg。
与跨国药企同台竞逐
根据高盛预测,2030年全球减肥药市场规模将达到1000亿美元。目前GLP-1市场由诺和诺德和礼来主导。
诺和诺德发布的2024年上半年财报显示,司美格鲁肽作为该公司的明星产品,上半年合计销售额达到129.6亿美元,同比增长43%。具体到不同版本,司美格鲁肽降糖注射版Ozempic销售额为82.87亿美元,同比增长36%;降糖口服版Rybelsus销售额为15.98亿美元,同比增长32%。
礼来公布的2024年上半年财报显示,替尔泊肽在降糖领域的销售额为48.974亿美元。替尔泊肽虽然进入市场时间晚,但迅速增长的销售额充分证明了GLP-1/GIP双靶点创新药的升级迭代优势,以及临床疗效和市场价值。
下一个挑战者会是谁?
GLP-1这一类药物一直都有“头对头”的传统,新产品基本会在临床三期直接“头对头”上一代最好的产品。从目前的临床进展来看,博瑞医药开展的2型糖尿病II期临床是国内为数不多的头对头司美格鲁肽。
数据显示,司美格鲁肽和替尔泊肽占据了目前整个GLP-1类市场80%以上的市场份额。在这种大环境下,谁能在临床头对头正面击败前者,谁就会是这个超千亿美元有力的竞争者之一。
根据公司此前在《NATURE》杂志子刊上刊登的论文,BGM0504基于人工智能和计算机模拟的分子优化设计,在相应的体内、体外试验中,其在GLP-1R/GIPR的激动活性上是替尔泊肽的3倍。这意味着BGM0504在分子动力学和药代动力学实验(非头对头)层面已经超过了替尔泊肽。现在,BGM0504降糖适应症II期数据的确在文献数据层面也超过了替尔泊肽。
根据针对替尔泊肽的SURPASS-1的研究数据,以及之前发表在国际期刊上的报告数据,按照最低剂量组5mg目标剂量治疗12周时,BGM0504的HbA1c较基线平均降幅(扣除安慰剂)为1.99%,明显优于替尔泊肽5mg治疗8周(1.14%)、26周(1.67%)和40周(1.7%)。可见,同样剂量,BGM0504降糖效果更好,且见效时间更短。
博瑞医药表示,BGM0504双靶点作用机制还使其在治疗肥胖症和非酒精性脂肪性肝炎(NASH)等代谢性疾病方面展现出巨大的潜力。公司将继续加大研发投入,推动BGM0504在多个适应症领域的临床研究和产业化进程。
中国市场潜力巨大
在中国市场,司美格鲁肽和替尔泊肽都已获批降糖和减重适应症。其中司美格鲁肽为降糖版司美格鲁肽注射液Ozempic、口服降糖版司美格鲁肽Rybelsus还在审批当中。
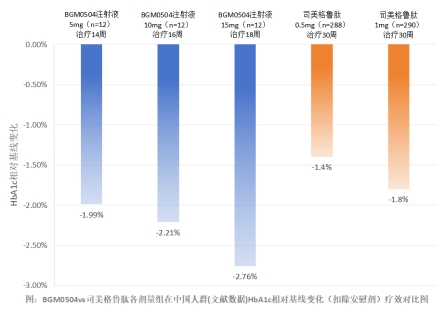
有关统计显示,仅2024年1-2月,司美格鲁肽在全国医保报销就超过了70万人次。然而,BGM0504vs司美格鲁肽各剂量组在中国人群(文献数据)HbA1c相对基线变化(扣除安慰剂)疗效对比显示,BGM0504呈现明显优势。若后续试验顺利、BGM0504推向市场后,有望抢占更大的市场份额。
博瑞医药2022年12月30日拿到新药研究申请(IND)批件。到今年6月份为止,仅用了18个月时间,BGM0504注射液就完成了从临床试验的获批到三期临床布局的开展。公司目前已经在生产制造端进行了超前布局。去年12月,博瑞医药拟新增3.5亿支/年BGM0504注射液产能,共3条产线,用途为“降糖、减肥”。
博瑞医药董事长袁建栋表示,公司将全力推进并完成III期临床研究,以期早日实现BGM0504的上市销售。