东海研究 | 深度:特宝生物(688278):乙肝临床治愈市场空间广阔,派格宾持续放量可期
(来源:东海研究)

证券分析师:
杜永宏,执业证书编号:S0630522040001
伍可心,执业证书编号:S0630522120001
联系人:
付婷,邮箱:futing@longone.com.cn
// 报告摘要 //

公司业绩增长强劲,股权激励目标高彰显发展信心。公司是国内重组蛋白长效制剂药物龙头企业,自1996年成立以来,围绕病毒性肝炎、恶性肿瘤及免疫治疗领域,前瞻性布局重组蛋白质及其聚乙二醇长效修饰平台,深耕重组蛋白药物开发。目前已上市5个产品,分别为派格宾、特尔立、特尔津、特尔康和珮金,均已纳入国家医保,核心产品派格宾在乙肝临床治愈领域表现优异,销售持续放量,带动公司收入快速增长。2018-2023年,公司营收从4.48亿元增至21.00亿元,年复合增速为36.19%,归母净利润从0.16亿元增至5.55亿元,年复合增速达103.28%。2024年8月,公司发布股权激励计划,考核以2023年度净利润为基数,2024-2026年业绩考核目标分别为年度净利润增长率不低于30%、70%、120%。公司未来三年业绩高增长目标明确,彰显公司长期发展信心。
抗病毒治疗人群不断扩大,派格宾有望持续放量。我国慢乙肝患者规模庞大,2022年我国HBV感染者达7974万人,其中慢性乙肝患者2000万人-3000万人。国内外权威防治指南均建议患者接受抗病毒治疗,临床治愈是理想治疗目标。派格宾是国内唯一上市的长效干扰素药物,广泛应用于乙肝临床治愈和降低乙肝相关肝癌发生风险的临床研究与实践,相关真实世界研究也在探索不确定期、非活动期等更多优势人群,PEG-IFN-α联合NAs用于追求临床治愈的初治或NAs经治优势人群将有望随之快速扩大。优秀的临床效果推动派格宾持续放量,2023年派格宾销售额17.90亿元,同比增长54.21%,对应覆盖患者约5万余人。目前派格宾渗透率仍较低,中短期内派格宾慢乙肝临床治愈基石地位稳固、国内竞争格局优异、集采风险较为可控、优势人群扩大,我们认为随着以派格宾为基础的乙肝临床治愈科学证据不断积累,派格宾的优势持续扩大,渗透率有望加速提升,市场空间广阔。
创新管线逐步进入收获期。长效G-CSF(珮金)于2023年6月上市并同年进入医保,公司已将该产品在中国大陆的独家推广销售权利授予复星医药,已获得7300万元的首付款和里程碑款项,复星强大的商业化能力有望助力珮金快速放量。2024年1月,长效重组人生长激素上市申请获受理,预计2025年上市,有望成为国内百亿生长激素市场第二家上市产品;重组人促红素正在开展III期临床研究申请相关准备工作,国内进度第三。人干扰素α2b喷雾剂、AK0706项目处于I期临床研究。外部合作方面,公司以有偿方式取得苏州康宁杰瑞重组人GLP-1/GIPR融合蛋白在非酒精性脂肪肝领域的独占许可权利,不断丰富公司产品管线等。
投资建议:公司核心产品持续放量,我们预计公司2024-2026年实现营收28.39/38.03/49.94亿元,实现归母净利润7.72/10.46/13.87亿元,对应EPS分别为1.90/2.57/3.41,对应PE分别为41.19/30.41/22.94倍。维持“买入”评级。
风险提示:行业政策变动风险;产品商业化不及预期风险;技术升级迭代风险。
// 正文 //

▌1.深耕长效重组蛋白领域,创新实力雄厚
1.1公司是不断成长的重组蛋白药物开发创新企业
特宝生物成立于1996年,主要从事重组蛋白质药物研发、生产及销售,以免疫相关细胞因子药物为主要研发方向,专注重组蛋白质及其长效修饰领域20余年。创始人孙黎先生早年间带领团队研发出特尔立、特尔津和特尔康三款短效改良型重组蛋白药物,打破了国外同类产品在国内市场的垄断地位,为公司重组蛋白质药物研发、生产领域奠定了坚实的基础。2005年公司从北京键凯科技引入Y型聚乙二醇(PEG)活性修饰剂的全球独家许可,形成了一系列长效PEG修饰核心技术。2016年,公司的首款长效重组蛋白I类新药长效干扰素(rhIFN-α2b)派格宾获批上市,2023年重组长效人粒细胞刺激因子(rhG-CSF)珮金上市,2024年重组长效怡培生长激素(rhGH)益佩生上市申请获受理。
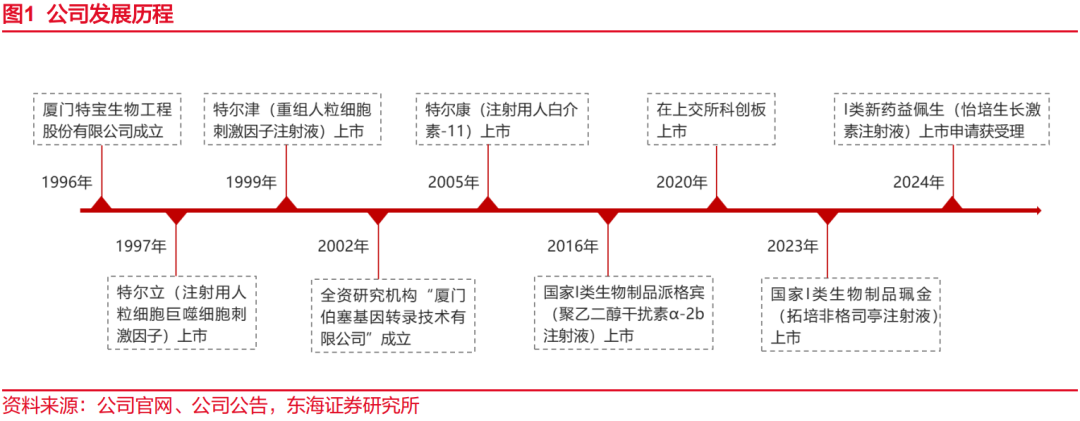
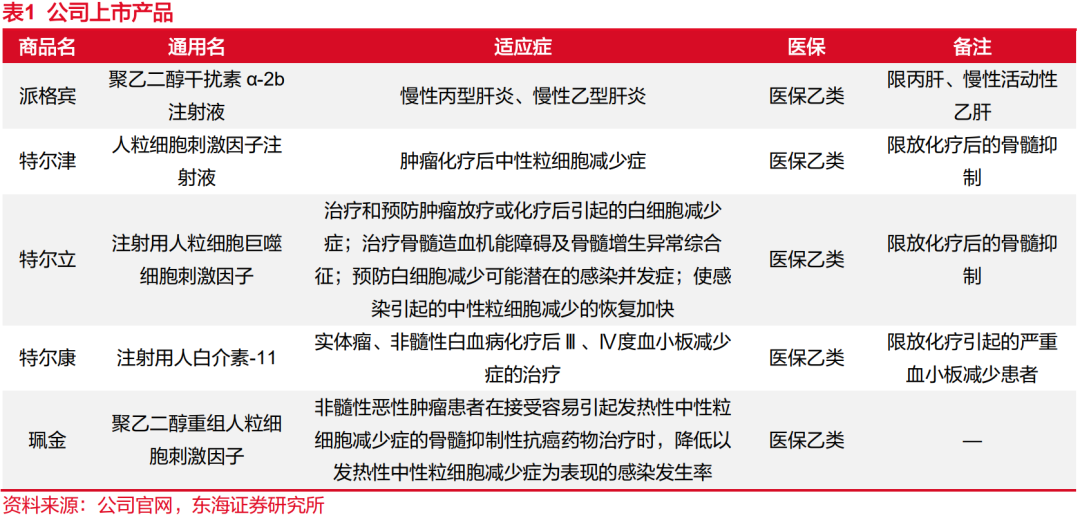
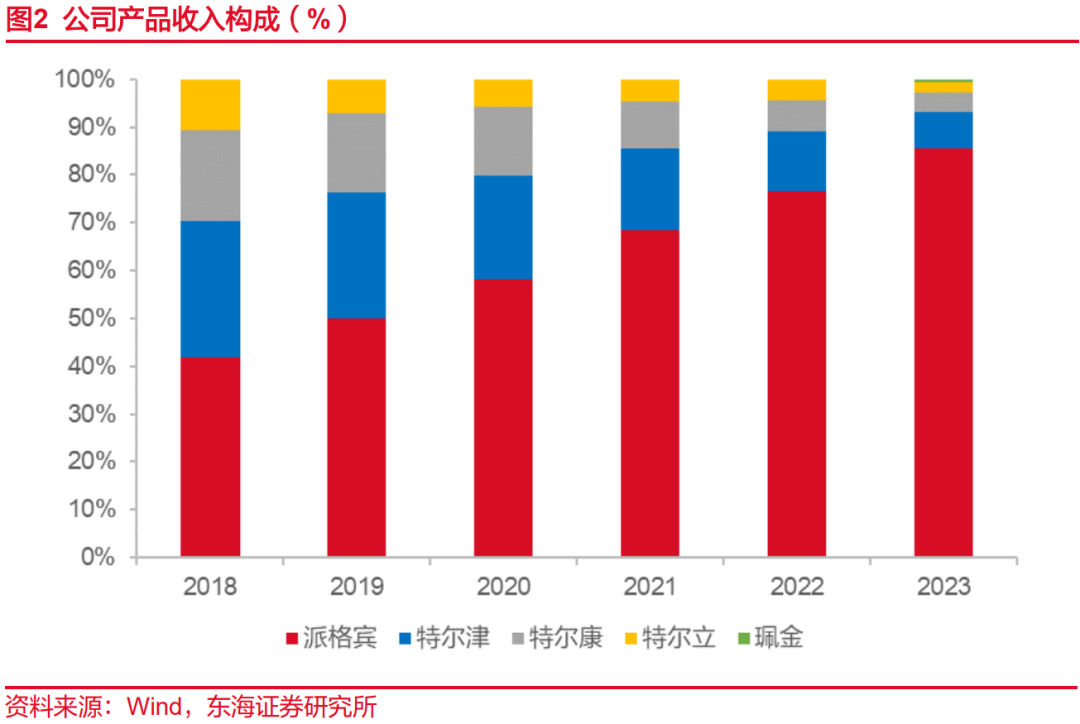
目前公司已上市5个产品,分别为派格宾、特尔立、特尔津、特尔康和珮金,均已纳入国家医保。派格宾为慢性乙型肝炎抗病毒治疗二线用药,与NAs(核苷(酸)类药物)联用为部分NAs经治优势患者追求乙肝临床治愈一线疗法,其与核苷(酸)类药物联合用于慢性乙肝临床治愈增加适应症上市申请已于2024年3月获NMPA受理。特尔津、特尔立、特尔康和珮金均属造血生长因子,对于肿瘤放疗、化疗过程中的不良反应发挥重要治疗作用。从公司产品收入构成上看,2018-2023年间,派格宾营收占比从42%快速上升至86%,成为公司拉动营收快速增长的主要产品。特尔津、特尔立和特尔康作为成熟产品,在造血生长因子细分市场份额领先,新产品珮金于2023年6月上市。
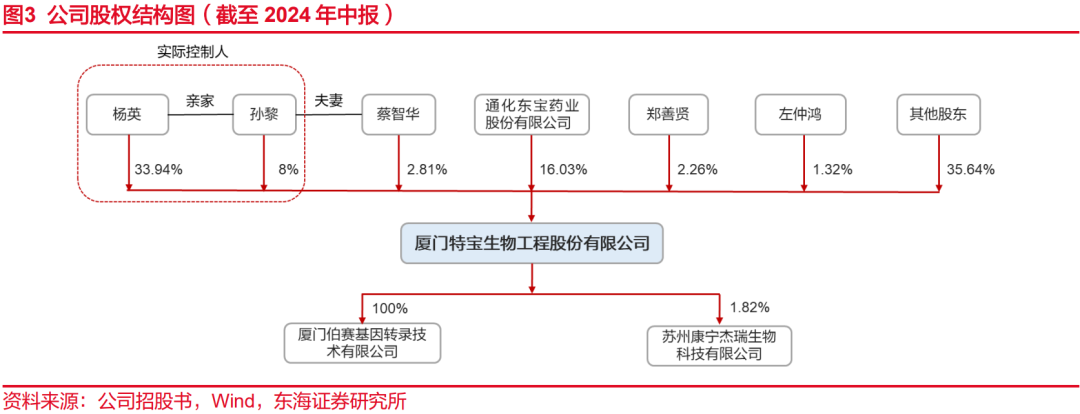
1.2公司股权稳定,实控人利益与公司高度一致
截至2024年中报,公司的实际控制人为杨英女士和孙黎先生,两人系亲家关系且为一致行动人,利益高度绑定,目前合计持股41.94%。杨英女士1997年入股特宝生物,入股以来不断增持,目前是公司第一大股东。第二大股东是通化东宝,持股16.03%,通化东宝所生产的药品与公司的药品针对的受众群体和适应症完全不同,不存在利益冲突。郑善贤、左仲鸿是公司共同创始人之一,分别持股2.26%、1.32%。孙黎先生是公司的共同创始人之一,自公司成立之日起即担任公司的董事,历任公司的总工程师、副总经理,自2013年5月起担任公司的总经理,现任董事长兼总经理。全面负责公司的经营管理工作,并且是公司的技术带头人,其工作内容对公司的经营发展起到非常关键的作用。
1.3收入利润快速增长,盈利能力持续提升
2018-2023年间,公司营业收入从4.48亿元增长至21.00亿元,CAGR达到36.19%;归母净利润从0.16亿元增长至5.55亿元,CAGR达到103.28%。2024H1,公司实现营业收入11.90亿元,同比增长31.68%,归母净利润3.04亿元,同比增长50.53%。公司收入和利润端均实现快速增长,业绩表现亮眼。
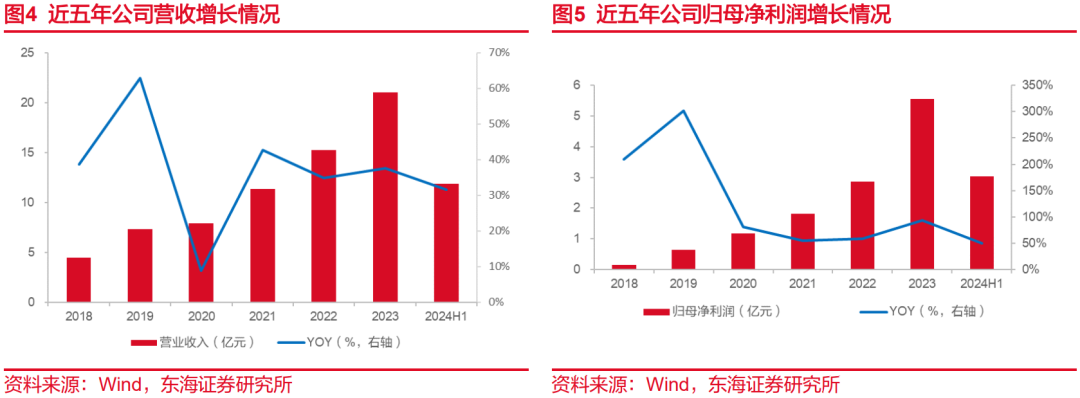
公司净利率不断提高,2018-2023年净利率从3.57%提升至26.45%,主要是收入规模的扩大带动销售费用率的摊薄。2018-2022年间,公司毛利率维持在87%-89%之间,2023年公司毛利率提升至93.33%,同比提高4.42pct,主要由于公司和键凯科技的PEG协议到期,公司不再支付相关的专利费用使得整体营业成本有所下降。2024H1,公司销售毛利率达到93.36%(同比增长0.42pp),销售净利率达到25.58%(同比增长3.2pp)。从费用上看,2018-2024H1年间,公司销售费用率从59.45%降至42.00%,管理费用率从11.99%降至10.04%,我们认为公司销售费用率和管理费用率还有一定下降空间,带动公司盈利能力持续提升。
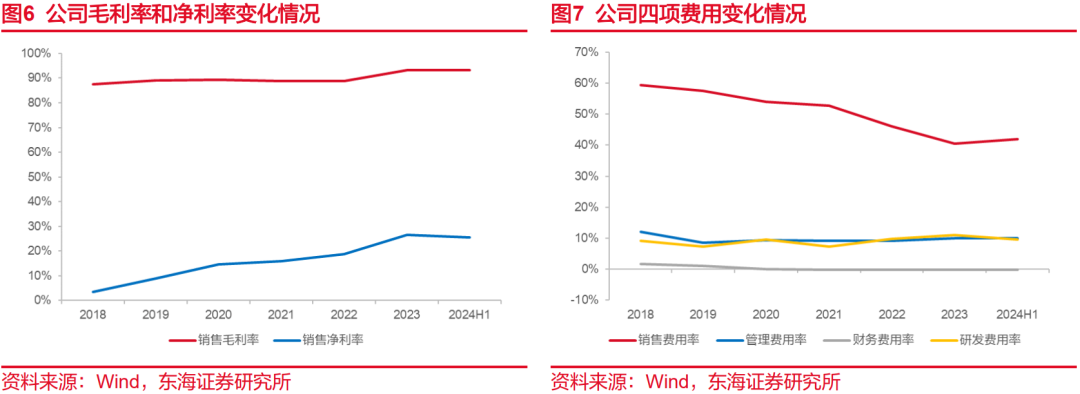
1.4研发投入持续加大,多项临床进展顺利
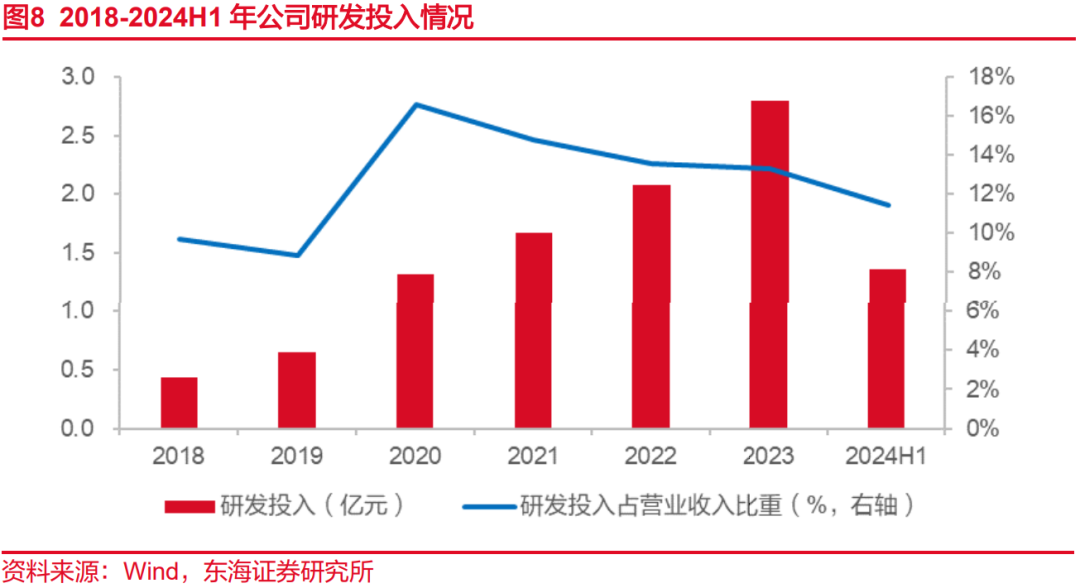
公司持续加大研发投入,从2018年的0.43亿元增至2023的2.80亿元,CAGR为45.23%;2024H1,公司研发投入1.36亿元,自主研发项目顺利推进。从在研管线上看,公司布局多款长效重组蛋白制品,2024年1月,Y型聚乙二醇重组人生长激素(YPEG-rhGH)NDA获受理,预计2025年上市。Y型聚乙二醇重组人促红素(YPEG-rhEPO)已完成II期临床,正在开展III期临床申请相关准备工作。随着在研管线的逐步推进,长效产品陆续上市有望对依从性较差的短效产品形成良好替代。在乙肝领域,在推进慢性乙型肝炎患者的临床治愈研究之外,公司积极探索不同机制药物的联合及更优的治疗方案。公司与爱科百发合作开展的乙肝新药AK0706已进入临床研究阶段,与Aligos Therapeutics签署利用核酸技术治疗肝炎的研究合作和开发协议,公司在乙肝治疗领域的研发管线布局不断拓展。
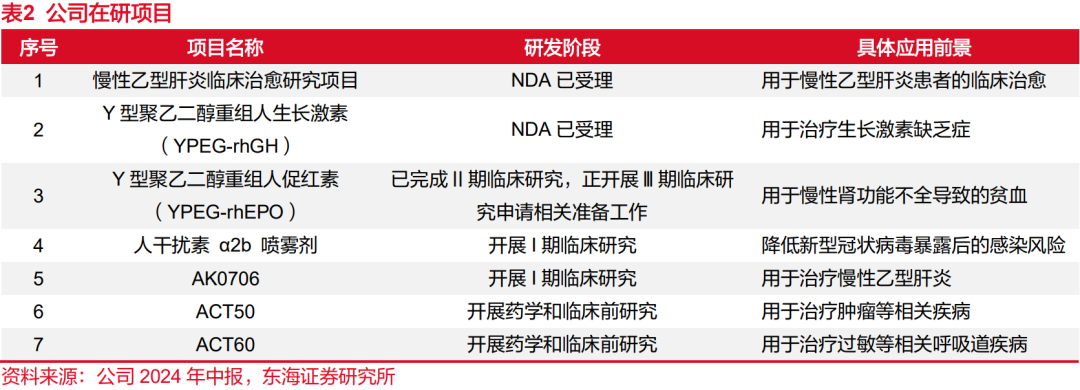
1.5股权激励彰显长期发展信心
2024年8月,公司发布股权激励计划,拟授予激励对象的限制性股票数量为600万股,占公司股本总额的1.47%,其中,首次授予480万股,占本激励计划草案公告时公司股本总额的1.18%,占本次授予权益总额的80%;预留120万股,占本激励计划草案公告时公司股本总额的0.29%,占本次授予权益总额的20%。授予的激励对象共计677人。考核年度为2024~2026年三个会计年度,以2023年度净利润为基数,2024-2026年业绩考核目标分别为年度净利润增长率不低于30%、70%、120%(净利润均指剔除股份支付费用后归属于上市公司股东的净利润)。公司股权激励目标高,彰显公司长期发展信心。
▌2.慢乙肝市场空间大,派格宾放量可期
2.1乙肝是全球性的卫生问题
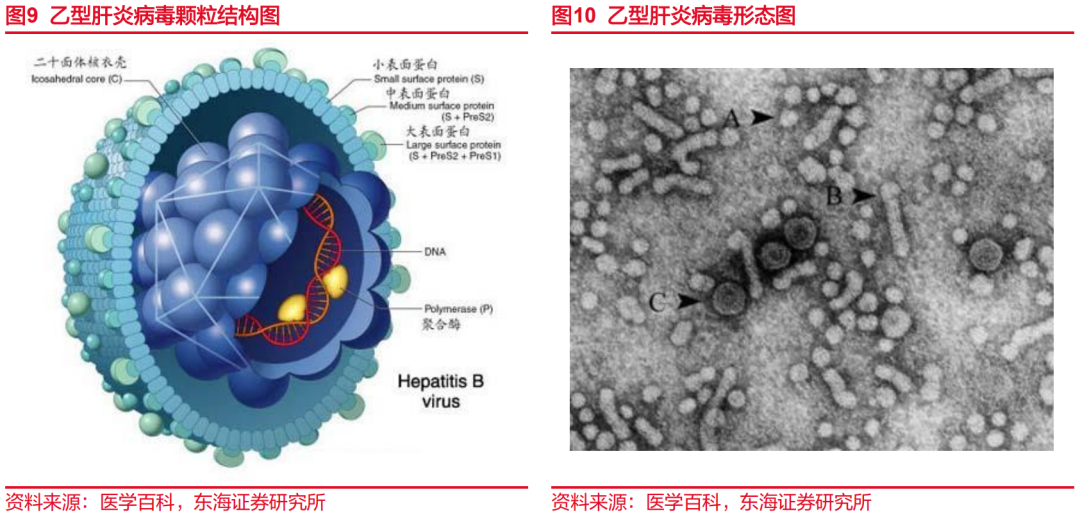
乙型肝炎病毒(Hepatitis B virus,HBV)属嗜肝DNA病毒科,是一种有囊膜的病毒,囊膜主要是由3种表面蛋白LHBs、MHBs和SHBs组成。核衣壳由核心蛋白(也称为乙肝核心抗原,HBcAg)形成,核衣壳包裹部分双链环状DNA基因组,基因组长约3.2kb,与病毒聚合酶共价连接。HBV对外界环境抵抗力较强,30-32℃可存活至少6个月,-20℃可存活15年,但65℃10小时、煮沸10min或高压蒸汽均可灭活HBV,环氧乙烷、戊二醛、过氧乙酸和碘伏对HBV也有较好的灭菌效果。大部分感染者体内HBV复制水平较高,具有传染性。从形态上看,乙型肝炎病毒有小球形颗粒、管形颗粒、大球形颗粒3种形态,直径约22nm的小球形颗粒是HBV后中最多见的一种,由HBsAg囊膜组成,管形颗粒是一串聚合起来的小颗粒,长度在100-700nm之间,大球形颗粒直径约42nm,由HBsAg囊膜和含有DNA分子的核衣壳组成。
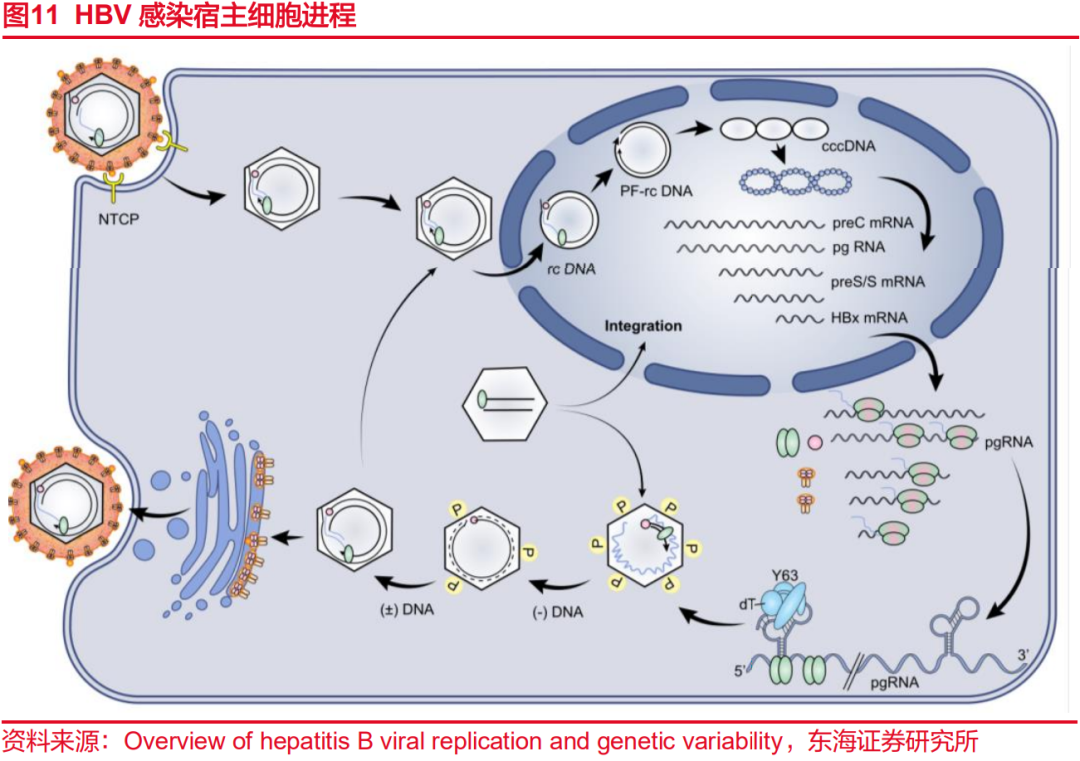
HBV通过肝细胞膜上的钠离子-牛磺胆酸-协同转运蛋白(Sodium taurocholate cotransporting polypeptide,NTCP)作为受体进入肝细胞,在细胞质中,HBV病毒褪去核衣壳释放松弛环状DNA(rcDNA),在细胞核内以负链DNA为模板形成共价闭合环状DNA(Covalently closed circular DNA,cccDNA)。cccDNA难以彻底清除,是导致慢性感染的重要机制之一。以cccDNA为模板转录而成的前基因组RNA(PregenomeRNA,pgRNA)是病毒逆转录的模板,在核衣壳中,pgRNA逆转录形成rcDNA,新合成的rcDNA可以进入细胞核进行新一轮的结构转变和复制转录,或被病毒外膜包裹形成完整子代病毒颗粒释放至血液中。
慢性乙型肝炎(Chronic Hepatitis B,CHB)是指由乙型肝炎病毒持续感染引起的肝脏慢性炎症性疾病。在复制过程中,除了形成cccDNA外,受感染肝细胞还不断地表达出一系列特定蛋白质,被人体免疫系统识别为抗原(包括HBeAg(e抗原)、HBsAg(表面抗原)等),人体免疫系统会启动清除抗原的机制,并不断攻击产生抗原的受感染肝细胞甚至正常的肝细胞,导致肝脏发生炎症。通常而言,在不接受抗病毒治疗的情况下,患者体内已有大量的受感染肝细胞,并持续不断有正常的肝细胞受到感染,而HBeAg、HBsAg等抗原还会通过进一步抑制人体免疫系统中相关免疫细胞的功能,抑制人体免疫系统的应答强度。上述过程导致人体的免疫系统难以及时、有效、全面地清除受感染肝细胞,造成肝脏炎症的持续恶化,最终将导致患者发生肝硬化和肝癌。
2.2我国是全球乙肝负担最大的国家
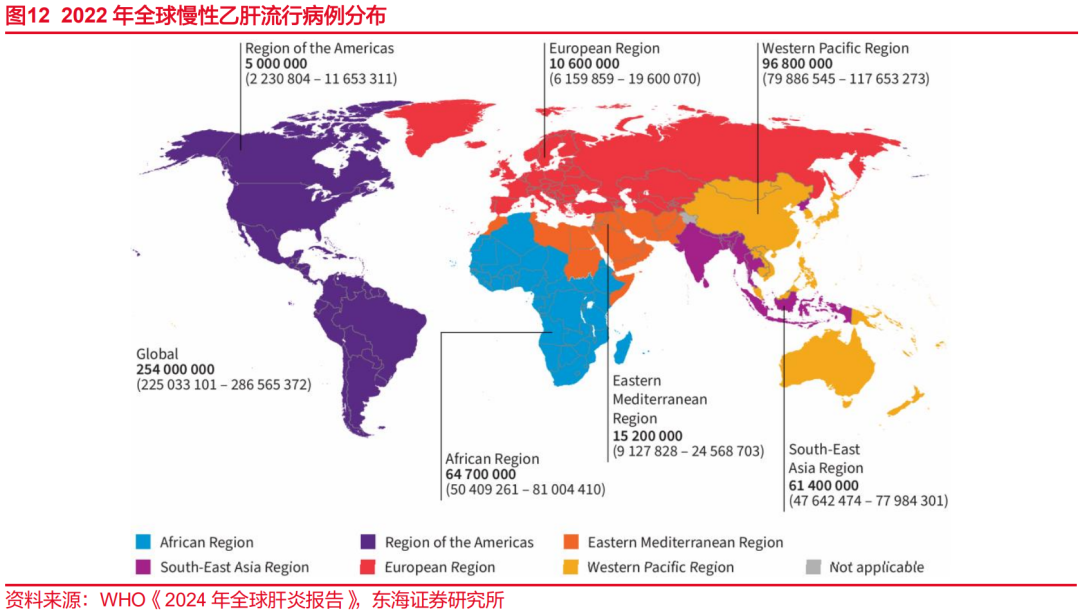
根据世界卫生组织《2024年全球肝炎报告》,HBV感染呈世界性流行,病毒性肝炎已成为仅次于结核病的全球第二大传染病“杀手”。2022年全球大约2.54亿慢性乙肝感染者,2022年新增120万例。2022年病毒性肝炎导致大约130万人死亡,其中83%的死亡病例由乙肝引起。受HBV感染发生年龄等因素影响,不同地区HBV感染的流行强度差异较大,西太平洋地区乙肝病例数最高,其次是非洲地区。
我国是乙肝大国,全球乙肝患者1/3在中国。据Polaris Observatory Collaborators公布数据显示,2022年我国HBV感染者达7974万人,其中慢性乙肝患者2000万人-3000万人。根据国家中国卫生健康统计年鉴数据显示,近十年来,我国每年报告的慢性乙型肝炎发病数均在100万左右。虽然我国乙肝疫苗的接种率在2013年就已经达到90%以上,可以有效预防新发感染,但是无法解决现有乙肝患者的问题。由于存量患者数字巨大,乙肝相关肝硬化、肝癌死亡人数仍呈现逐年增加趋势。
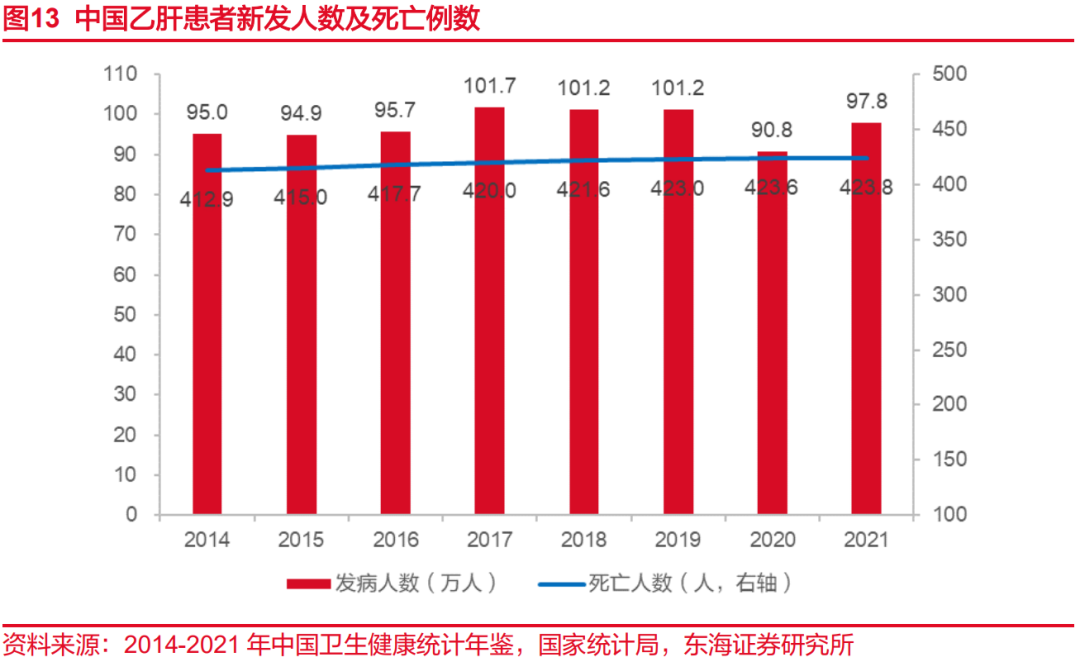
与发达国家相比,中国HBV患者诊疗率、治疗率仍有较大差距。根据2018年发表于The Lancet Gastroenterology & Hepatology的数据显示,全球乙肝发病率约为4.9%,中国的历史发病率较高,并且诊断率及治疗率与发达国家有较大的差距。这导致很多存量病人没能得到很好地治疗,发展为肝硬化甚至肝癌。随着国家政策的推动与支持,抗病毒药物可负担性与可及性不断提高,我国HBV感染诊疗取得巨大进步,但目前HBV感染者诊断率和治疗率分别为24%和15%,与WHO提出的“至2030年肝炎病毒诊断率和治疗率分别达到90%和80%”仍有较大差距。由此可见,我国HBV药物市场有着极大需求。
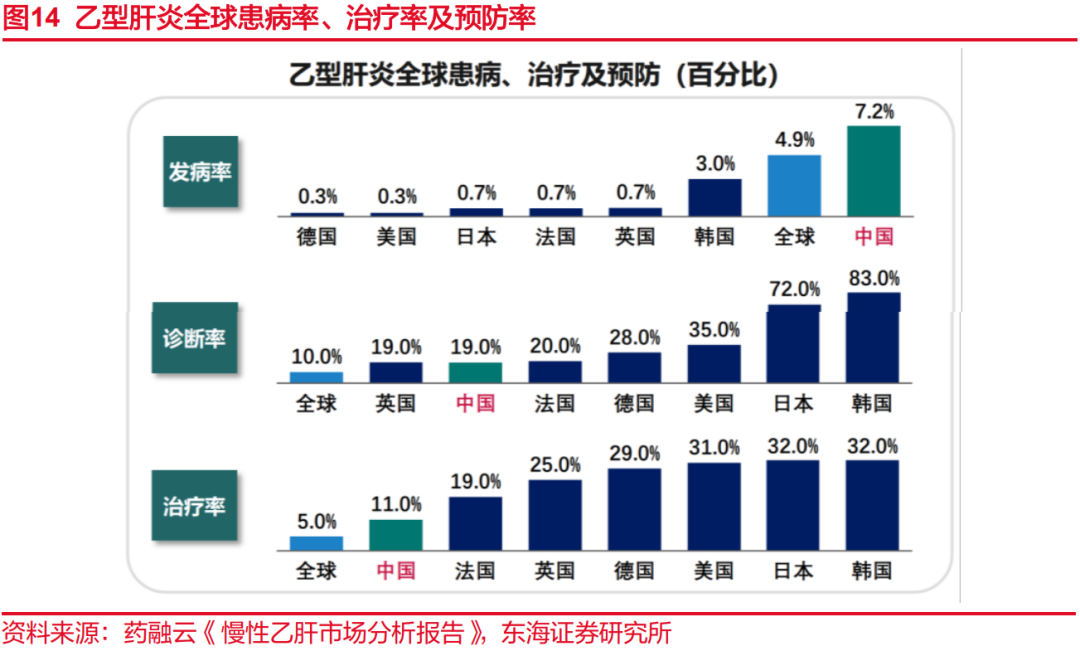
2.3临床治愈明确,长效干扰素效果好
2.3.1.临床治愈已成为国内外指南推荐理想治疗目标
大多数HBV感染者最终会发展为慢性肝炎和肝硬化阶段。HBV感染时的年龄是影响慢性化的最主要因素,在围生期和婴幼儿时期感染HBV者中,分别有90%和25%~30%将发展成慢性肝炎,而5岁以后感染者仅有5%~10%发展为慢性肝炎。同时,慢性肝炎会大幅增加未来罹患肝硬化和肝癌的风险,慢性乙肝患者肝硬化的年发生率为2%~10%,代偿期肝硬化进展为肝功能失代偿的年发生率为3%~5%,失代偿期肝硬化5年生存率仅为14%~35%。此外,非肝硬化的慢性乙肝感染者的肝癌年发生率达到0.5%~1.0%,肝硬化患者肝癌年发生率则高达3%~6%,肝癌患者5年生存率仅为10.1%。
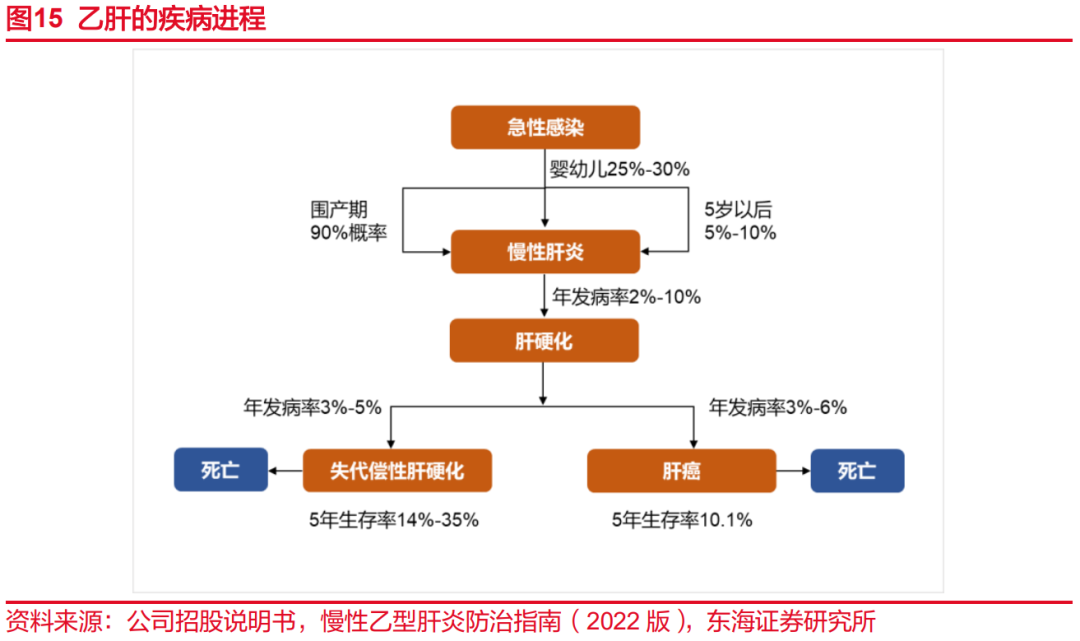
慢性乙肝临床治愈得到广泛的认可与提升。由于慢性乙肝在一定程度上会进一步发展为肝硬化和肝癌,并严重影响患者的生存时间和生存质量,国内外权威慢性乙肝防治指南均建议患者接受抗病毒治疗。CHB治愈分为完全治愈和临床治愈(功能性治愈)。完全治愈即血清HBsAg检测不到,cccDNA和整合HBV DNA被清除。由于cccDNA转录受到宿主细胞表观遗传机制的调节而稳定存在,目前缺少特异性靶向cccDNA的药物,完全治愈较难实现。临床治愈是国内外目前CHB防治指南公认的理想治疗目标,定义为停止治疗后HBsAg持续阴性,伴或不伴抗-HBs出现,HBV DNA低于最低检测下限,肝脏生物化学指标正常,肝细胞内仍存在cccDNA和整合的HBV DNA。
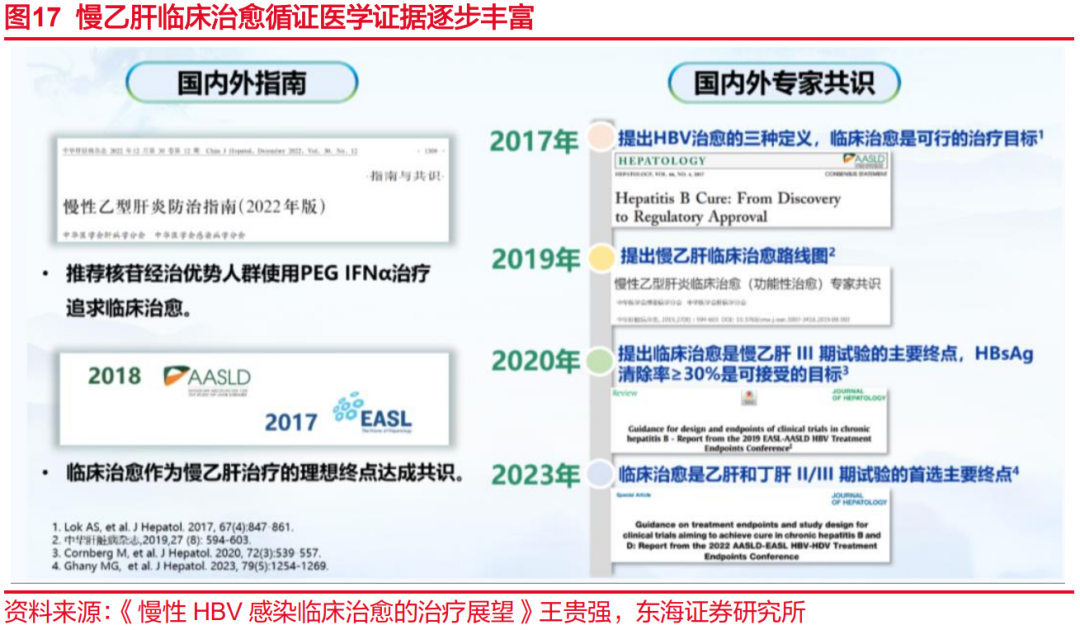
指南方面,在我国《慢性乙型肝炎防治指南》(2015年版)中包括3个治疗终点:基本的治疗终点、满意的终点和理想的终点,获得理想的终点相当于实现慢性乙肝临床治愈。研究显示,实现理想的治疗终点、满意的治疗终点、基本的治疗终点及未进行抗病毒治疗的5年肝癌发生率存在显著差异,更高的治疗终点,尤其是理想的治疗终点将大幅度降低患者的未来肝癌发生风险。在《慢性乙型肝炎防治指南》(2019年版)的“治疗目标”章节中,强调针对部分适合的患者,应追求临床治愈,说明临床治愈已逐渐成为一线治疗中追求的核心治疗终点。我国《慢性乙型肝炎防治指南》(2022年版)中已经将核苷(NAs)经治优势人群采用聚乙二醇干扰素α(PEG-IFNα)追求临床治愈写入推荐意见,得益于我国在NAs经治人群临床治愈方面取得的丰硕实践成果。美国肝病研究协会(AASLD)和欧洲肝病学会(EASL)指南也均将临床治愈作为慢乙肝治疗的理想终点。共识方面,从2017年国外专家对临床治愈是可行的治疗目标达成共识,2019年我国专家发布了慢乙肝临床治愈专家共识,提出慢乙肝临床治愈路线图。2020年EASL-AASLD对于乙肝III期临床试验的主要终点应该是临床治愈(功能性治愈),HBsAg清除率≥30%是可接受的目标达成共识。2023年EASL-AASLD就临床治愈作为乙肝或丁肝Ⅱ/III期试验的首选主要终点达成共识。国内外乙肝指南与共识的不断更新,体现了乙肝临床治愈受到越来越多的关注和认可。
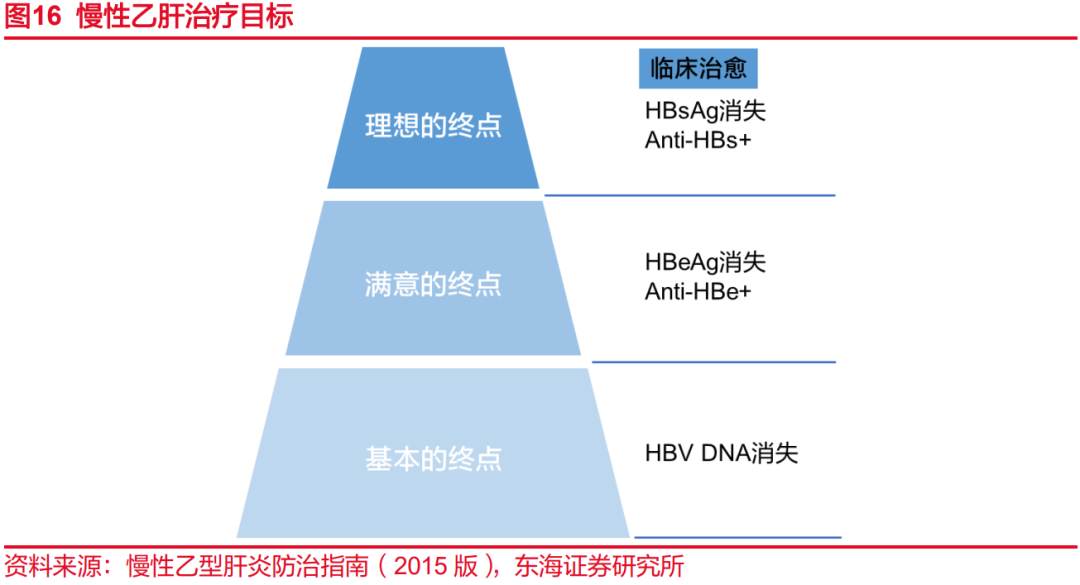
2.3.2.我国抗乙肝病毒药物治疗
在慢性乙肝治疗过程中,包括三组重要的检测指标体系,即HBV血清学检测、HBV基因检测和生物化学检测。
(1)血清学检测:HBV有三种抗原成分,分别是表面抗原(HBsAg)、e抗原(HBeAg)和核心抗原(HBcAg),这三种抗原在人体内可引起机体免疫反应,产生相应的三种抗体,即抗-HBs(HBsAb)、抗-HBe(HBeAb)和抗-HBc(HBcAb)。这些抗原和抗体可作为乙肝病毒感染的诊断标志。但由于用一般的方法在血清中很难检测到HBcAg,只能检测出HBsAg和抗-HBs、HBeAg和抗-HBe以及抗-HBc五项指标,所以我们习惯称之为“乙肝五项”或乙肝“两对半”。
(2)基因检测:核心检测指标包括HBV DNA定量(即乙肝病毒DNA水平定量值)等,主要用于评估慢性乙肝感染的病毒复制强度,是抗病毒治疗适应症及疗效判断的重要指征。
(3)生化检测:核心检测指标包括血清ALT和AST,主要用于反映肝细胞受损程度。

结合感染乙肝病毒过程,为了实现延缓和减少肝硬化、肝癌的发生风险,慢性乙肝患者的治疗核心机制主要包括两方面,一是抑制乙肝病毒复制强度,降低正常肝细胞进一步感染的风险;二是尽可能清除体内受感染的肝细胞,降低cccDNA表达水平。根据《慢性乙型肝炎防治指南》推荐,目前乙肝治疗药物主要包括核苷(酸)类似物和干扰素。
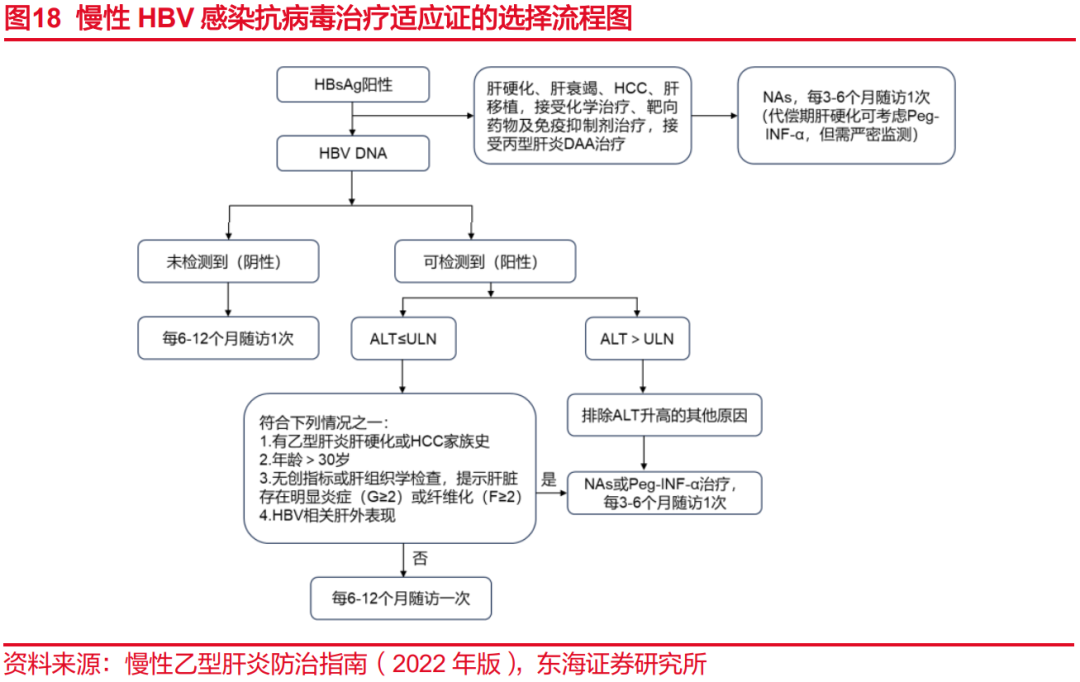
核苷(酸)类似物是一种经过人工修饰的核苷(酸),它的作用机制是通过抑制HBV DNA聚合酶的活性来抑制病毒复制,常见药物为恩替卡韦、替诺福韦二吡呋酯、丙酚替诺福韦等。干扰素的作用机制是通过与细胞表面的干扰素受体结合,诱导细胞产生抗病毒蛋白,从而抑制细胞复制,常见药物为聚乙二醇干扰素α。基于不同的作用机制,核苷(酸)类药物和聚乙二醇干扰素α在主要治疗终点、用药方面(给药方式、疗程)和不良反应方面也存在较大差异。核苷(酸)类药物以实现患者基本的治疗终点(即控制病毒复制水平)为主要目标,聚乙二醇干扰素α以实现更高的治疗终点(包括实现安全停药,实现e抗原血清学转换和临床治愈)为主要目标。
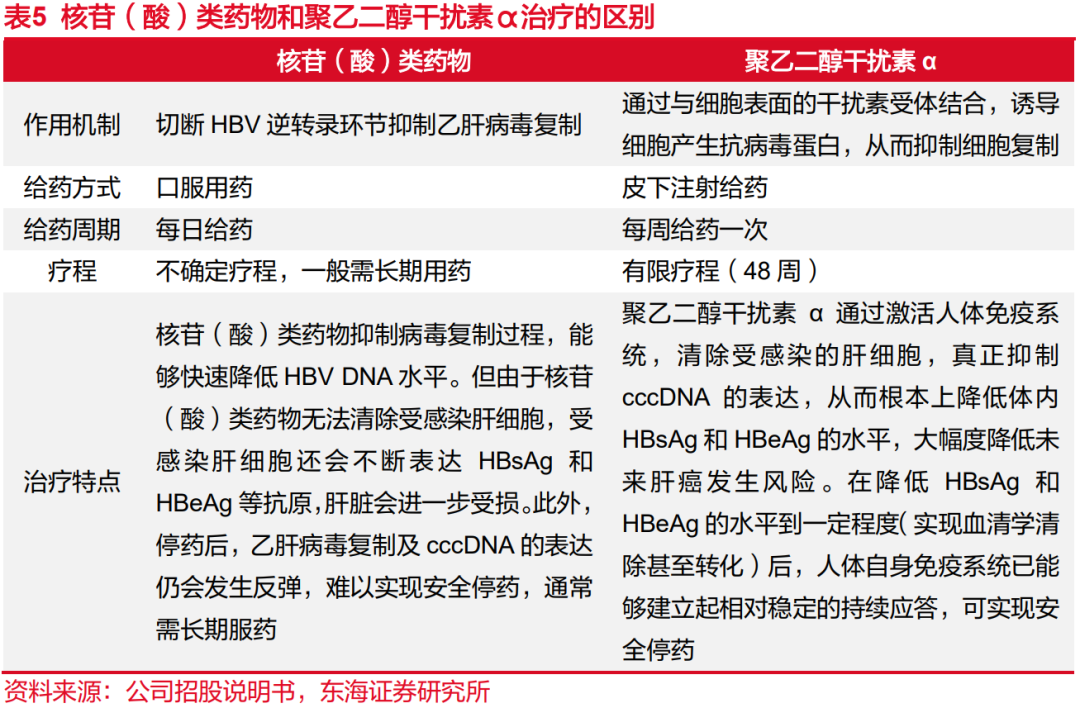
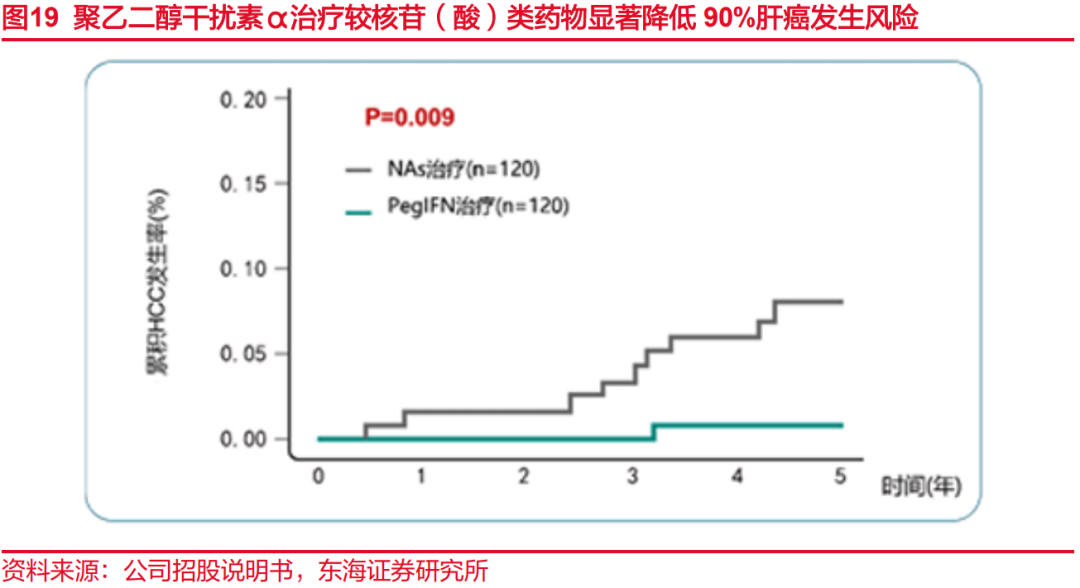
聚乙二醇干扰素治疗慢乙肝降低约90%的肝癌发生风险。在《中国慢性乙型肝炎防治指南(2019年版)》中,新增了聚乙二醇干扰素α进一步降低肝硬化、肝癌的发生率的循证医学证据:119对单独应用聚乙二醇干扰素α或恩替卡韦治疗并随访5年的数据发现,应用聚乙二醇干扰素α治疗的患者5年内均未发生肝癌;而恩替卡韦治疗者在随访第4、5年时分别有2例、1例肝癌,与模型预测发生率间无显著差别。另一项包括682例应用核苷(酸)类药物,430例应用干扰素单独或联合核苷(酸)类药物治疗的回顾性研究提示,在中位随访5.41年间共31例发生肝癌,接受干扰素治疗患者的10年累积肝癌发生率明显低于核苷(酸)类药物治疗患者(2.7%vs8.0%)。研究表明,与核苷(酸)类药物相比,聚乙二醇干扰素α在降低乙型肝炎病毒相关肝癌发生率方面的作用显著。
单药疗效有限,联合用药疗效更佳。在临床实践中,运用两类药物的抗病毒治疗方案通常包括单药治疗方案和联合治疗方案。单药治疗方案就是单独使用两类药物,由于NAs在HBV DNA清除上表现更好,且价格低、广谱性远强于长效干扰素,因此即使NAs需要长期服药,其依旧是一线CHB治疗的首选。联合治疗方案是联合(或序贯)核苷(酸)类药物和长效干扰素两类药物的联合治疗方案。根据近年来大量NAs序贯长效干扰素的临床数据读出,研究者发现联合用药方案能够将HBsAg清除率从NAs或干扰素单药的3%-11%,提升到接近30%,部分优势患者的清除率能够达到80%,提升了患者的治愈机会,该方案的应用也逐渐在临床一线开展。
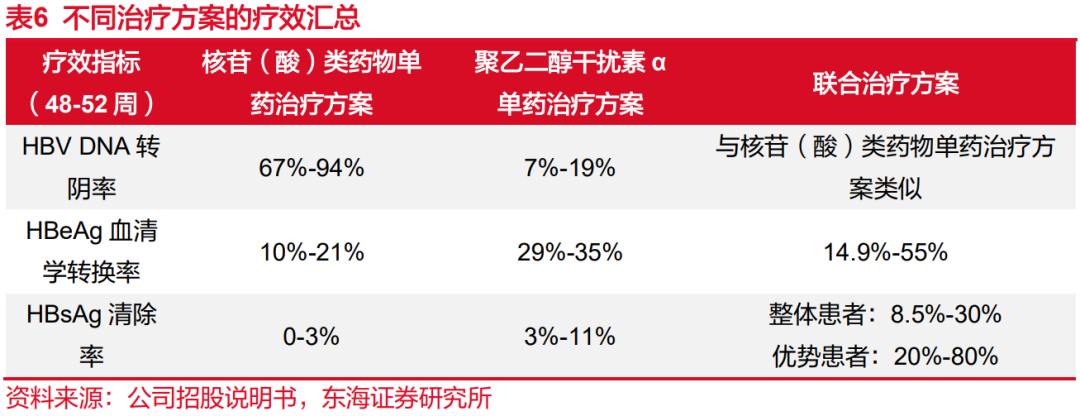
2.4长效干扰素渗透率低,派格宾放量空间大
2.4.1.派格宾是目前国内长效干扰素市场唯一产品
长效和短效干扰素在我国早期用于治疗CHB,2015年短效干扰素由于疗效不足退出指南后,临床上基本上仅用长效干扰素作为CHB治疗手段。在我国获批用于慢性乙肝治疗的长效干扰素只有公司的派格宾、罗氏的派罗欣和默沙东的佩乐能三个产品,默沙东的产品注册文号已到期,罗氏在2022年底收回了派罗欣的商业运营权。考虑到国内目前尚未有其他品牌长效干扰素获批上市,凯因科技的派益生(培集成干扰素α-2注射液)正在开展联合核苷(酸)类药物乙肝治愈的III期临床试验,这表明在其他产品获批上市前,派格宾将成为国内长效干扰素市场唯一产品,享有一定时间的市场独占期。
派格宾是孙黎先生及其研发团队历时14年潜心研发的国产第一个拥有自主知识产权的长效干扰素α-2b,主要适用于治疗慢性乙型肝炎和慢性丙型肝炎,其相关两个结构专利已获得中国、美国、欧洲和日本等30多个国家授权,其药物研发及相关临床应用得到了“十一五”、“十二五”、“十三五”共4项重大新药创制国家科技重大专项的持续支持。派格宾的成功上市,打破了进口同类药物长期垄断,大幅度降低我国肝炎患者的用药成本,具有较好的经济效益和社会效益。
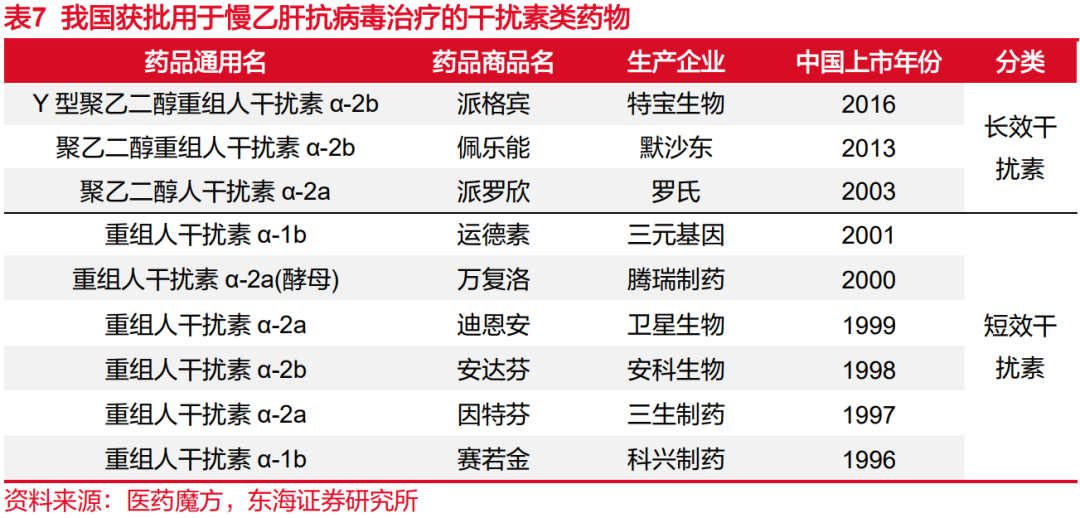
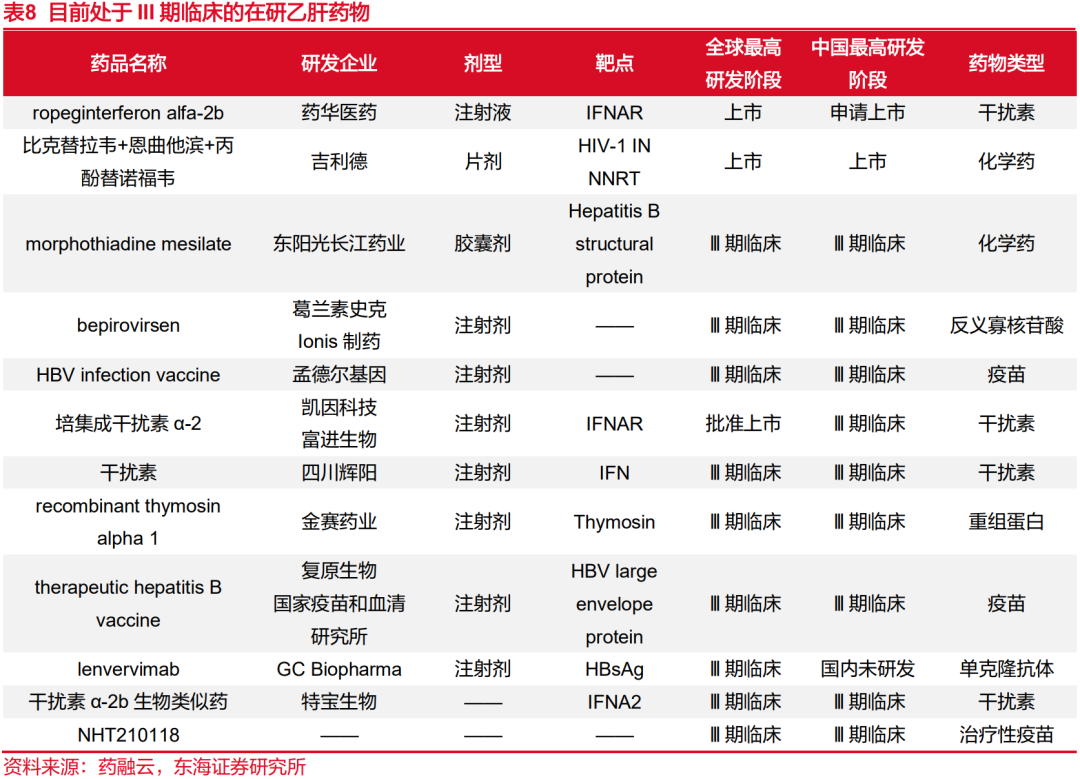
近年来受集采所带来的药物降价影响,我国乙肝病毒药物的市场规模有所萎缩,基本处于百亿元级别。由于核苷(酸)类药物为口服用药、不良反应较少且产品单价较低,目前在临床一线应用更为广泛,市场份额占比显著大于聚乙二醇干扰素α。2023年核苷(酸)类药物在抗乙肝病毒药物市场份额超2/3。
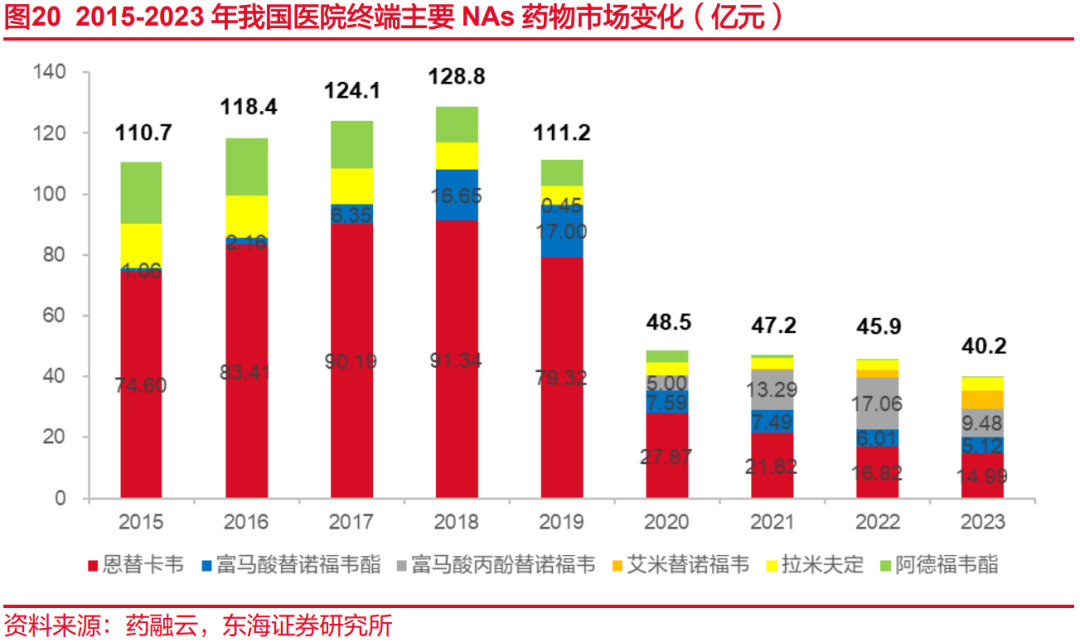
受益于良好的竞争格局,派格宾的市场份额逐年增高。根据药融云全国医院销售数据,在派格宾上市以前,进口长效干扰素占据着较大的市场份额,2016年度派罗欣和佩乐能的销售规模分别为7.01亿元和3.27亿元,占据了近乎全部的市场份额。派格宾于2016年底获批上市,2018年度的销售规模破1亿元,增长迅速,2023年达11.6亿元,在长效干扰素的市场规模的占比超94%。
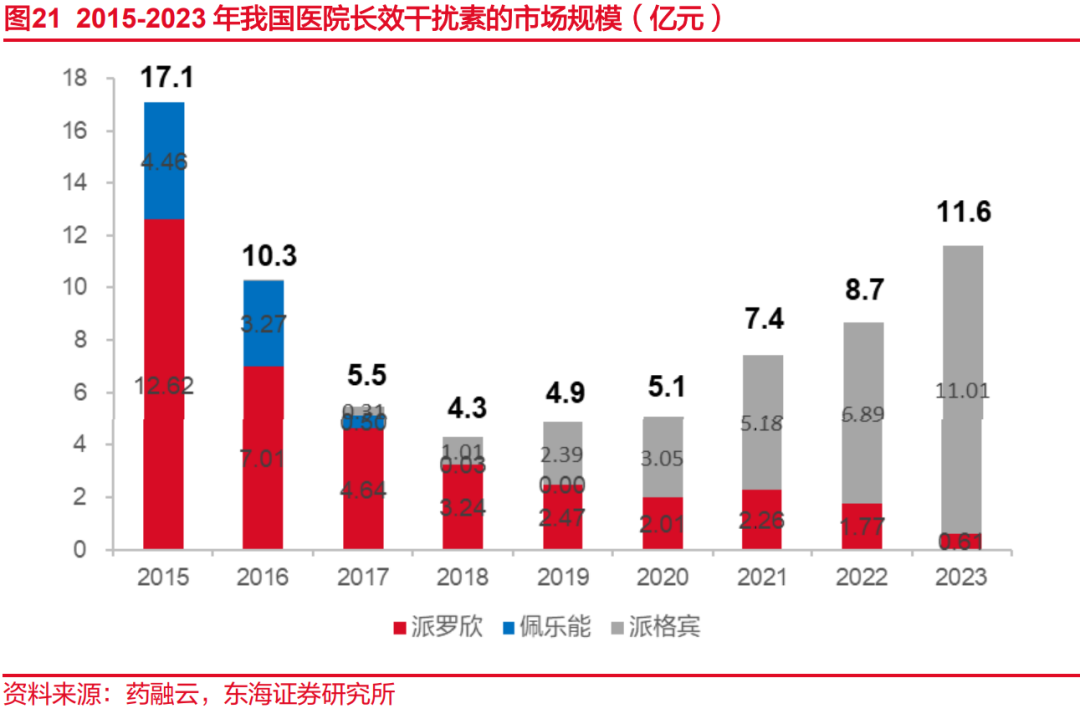
派格宾渗透率较低,具有较大提升空间。在我国现有的约8000万乙肝病毒携带者中,有2000-3000万人需要治疗,乙肝过去是被普遍认为无法治愈的,要终生携带病毒,但随着医药科技的进步和治疗观念的改变,现在乙肝临床治愈的概念已被广泛认可。目前,全国已有部分医院开通了乙肝临床治愈门诊。根据公司公告,派格宾在药品集中招标采购中的中标价格区间为697-667元/支,按照48周作为长效干扰素的完整治疗周期,一个完整治疗周期对应的用药费用为3.20万元-3.35万元。派格宾2023年销售额为17.90亿元,对应覆盖患者人数为5.34万-5.59万之间(假定所有患者均完成完整治疗周期),占国内慢性乙肝患者总人数和每年度新增的乙肝发病数的比重仍较低,具有较大的市场潜力。
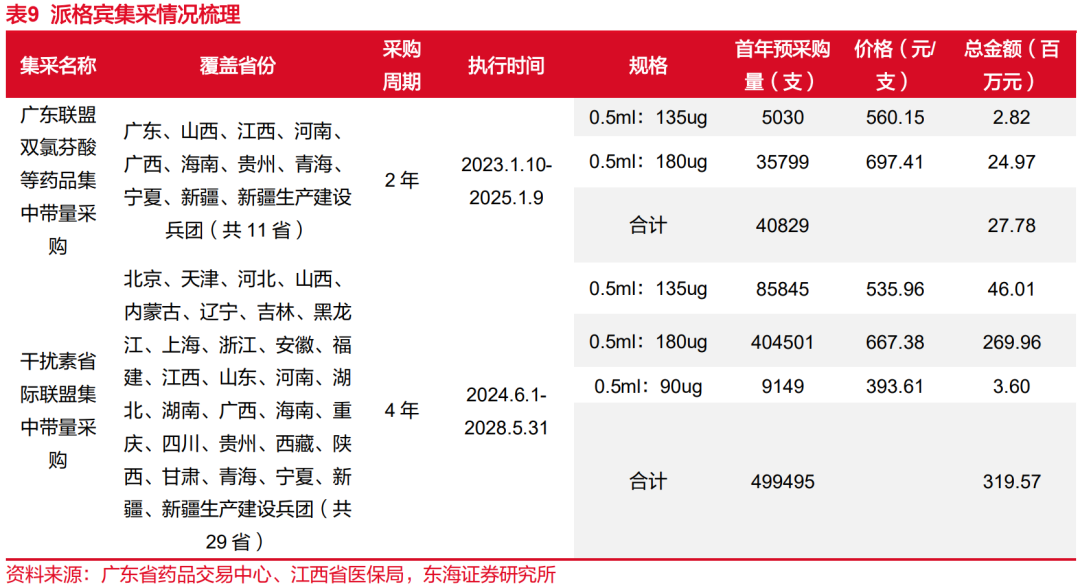
派格宾集采价格降幅温和,短期集采风险较为可控。聚乙二醇干扰素α2b在广东联盟双氯芬酸等药品集采和江西省牵头的干扰素省际联盟集采中被纳入。从价格来看,派格宾在两次集采中分别降价约15.0%和18.7%,广东联盟集采中180ug剂量的价格从820元/支下降至697元/支,江西省集采中进一步下降至667元/支,整体降幅温和。广东省集采已于2023年1月10日开始执行,江西联盟集采已覆盖29省,采购周期为4年,已于2024年6月1日起执行,预计未来四年派格宾不会有其他大型集采,集采风险较为可控。
2.4.2.抗病毒治疗人群持续扩大,派格宾不断被认可
抗病毒治疗人群不断扩大。随着对乙肝治疗研究认知的加深,近年来指南不断放宽相关指标限制,治疗范围从扩大CHB患者开始,逐渐拓展至免疫耐受期、非活动期。根据《慢性乙型肝炎防治指南(2022)》,可将乙肝携带者分为免疫耐受期、免疫清除期、非活动期、再活动期和不确定期五个分型。免疫清除期和再动活动期患者均为慢性乙肝(CHB)患者,该类患者肝细胞长期受损,更容易发生肝硬化(2%-10%)从而导致肝癌(3%-6%),死亡风险较大,国内外慢性乙型肝炎指南抗病毒治疗适应证主要是针对HBeAg阳性或阴性的慢性乙型肝炎或肝硬化患者,对免疫耐受期和非活动期一般不推荐治疗。不确定期是指部分未经治疗的慢性HBV感染者随访1年,按其HBV DNA、ALT水平及组织学均难以明确归于以上4期,约占28%-55%。不确定期患者并不是指他们处于一个独立的期,而是指他们难以被明确分期。相较于真正的慢性HBeAg阳性感染者(免疫耐受期)或HBeAg阴性的HBV感染者(非活动期),不确定期患者疾病进展风险仍然较高,因而可能也需要抗病毒治疗。2022年庄辉院士起草的《扩大慢性乙型肝炎抗病毒治疗的专家意见》提出对不确定期慢性乙肝患者进行抗病毒治疗;2024年2月,李兰娟院士起草的《乙型病毒性肝炎全人群管理专家共识(2023)》为《慢性乙型肝炎防治指南(2022)》未覆盖的免疫耐受期、特殊人群等患者首次进行指南指导,并指出要进一步简化抗病毒治疗适应症,扩大筛查,实现早诊断早治疗,全程管理。

各类慢乙人群临床治愈研究不断深入,派格宾的疗效和安全性得到更广泛验证。随着多项确证性临床研究的证明,我国已陆续启动多项真实世界大型研究,包括2018年由卫健委下属中国肝炎基金会开展的珠峰计划、绿洲计划等大型真实世界研究,深入探索乙肝临床治愈方案的优化。这些真实世界研究项目进一步证明NAs+长效干扰素的有效性,在提升患者对乙肝治疗的认知、优化和完善临床治愈路径、优化慢性乙型肝炎抗病毒治疗方案等方面发挥了重要作用,慢乙肝临床治愈正向着扩大抗病毒治疗人群,拓展临床治愈人群的新阶段发展。
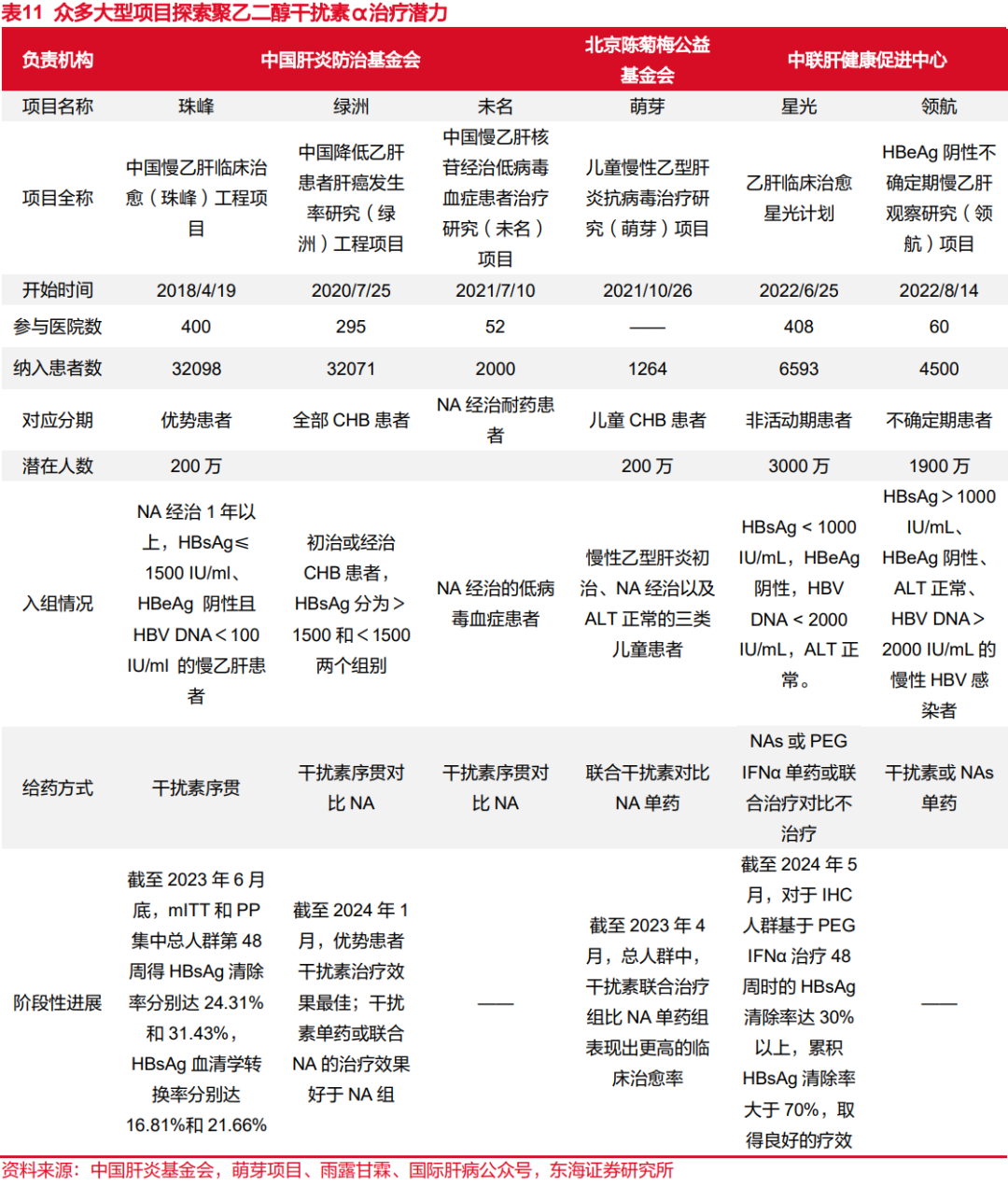
基于抑制病毒复制和增强免疫的双重作用,派格宾临床上主要用于病毒性肝炎的治疗,该聚乙二醇干扰素α-2b品种为现行国家医保目录(乙类)品种。随着中国《慢性乙型肝炎防治指南》(2022年版)将核苷经治慢性乙型肝炎患者的临床治愈写入推荐意见,临床治愈的观念得到进一步普及,具备临床治愈实践经验的医生数量逐步增加,派格宾的疗效和安全性得到更广泛地验证。目前,派格宾在实现慢性乙型肝炎患者临床治愈和预防肝癌方面开展了一系列研究工作,公司持续参与了多项乙肝临床治愈及肝癌预防真实世界研究项目,包括:“珠峰”项目(优势患者)、“绿洲”项目(全部CHB患者)、“未名”项目(NA经治耐药患者)、“萌芽”项目(儿童CHB患者)、“星光”计划(非活动期患者)、“领航”项目(不确定期患者)等。目前多个大型研究项目已经完成入组,临床研究成果有望持续落地,有望推动慢乙肝治愈医患教育进一步拓展,带动长效干扰素进一步放量。
▌3.其他长效重组蛋白产品渐入收获期
3.1长效G-CSF市场竞争激烈,公司长短效产品组合优势明显
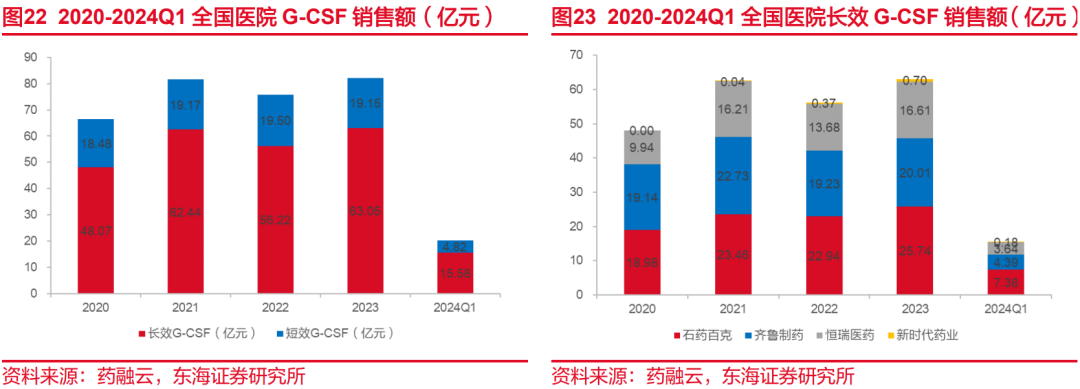
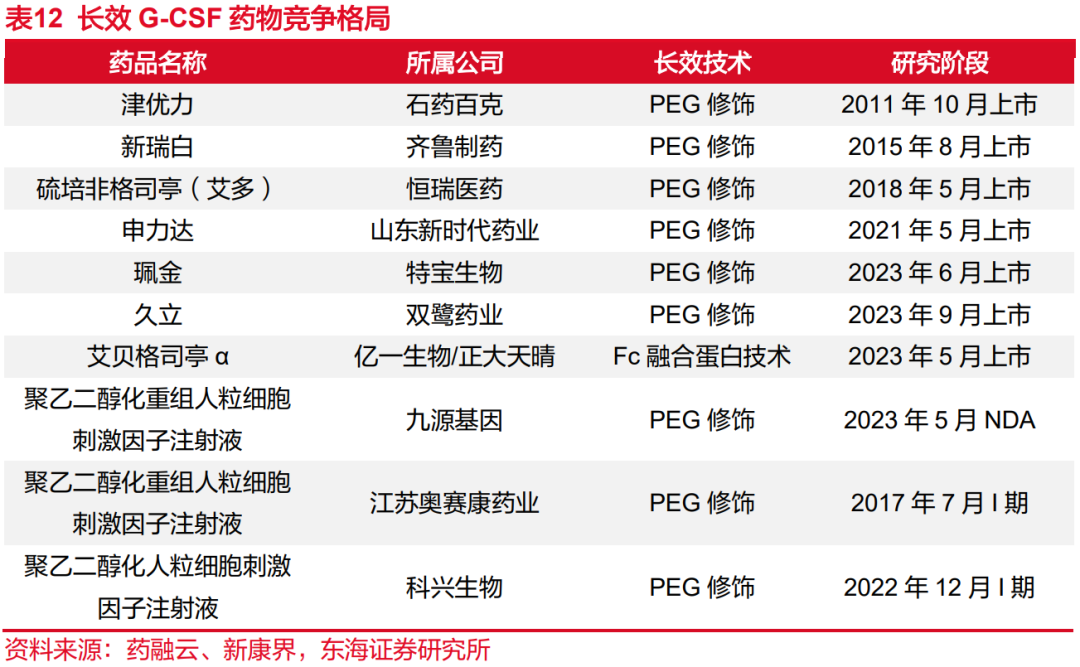
长效G-CSF优势明显,市占率高。粒细胞集落刺激因子(G-CSF)能够促进中性粒细胞增殖,用于提高肿瘤放化疗后白细胞和中性粒细胞的数量。G-CSF是国内外临床指南首推的放化疗相关中性粒细胞减少症药物,包括短效和长效两种类型,常用的长效G-CSF主要有聚乙二醇化重组人粒细胞刺激因子注射液(PEG-rhG-CSF),短效G-CSF主要有重组人粒细胞刺激因子注射液(rhG-CSF)。其中短效G-CSF在每个化疗周期内需要每日给药1~2次,而聚乙二醇化G-CSF在一个化疗周期中往往只需给药1次即可明显提升中性粒细胞水平,更为便捷。从全国医院销售数据来看,长效G-CSF自2011年上市以来市场快速增长,2023年销售额超63亿元,占比达76.7%。
珮金竞争优势突出,有望快速放量。目前国内已上市7个长效产品,其中6个使用了聚乙二醇(PEG)修饰技术。从竞争格局的角度来看,石药百克、齐鲁制药、恒瑞医药上市时间较早,占据几乎全部市场份额。新时代药业是2021年获批的,特宝生物、双鹭药业、亿一生物/正大天晴则是2023年最新获批的。公司拓培非格司亭注射液(珮金)于2023年6月上市并于同年进入医保,为Y型聚乙二醇修饰的人粒细胞刺激因子,与目前已上市的同类长效产品相比,珮金具有较长的药物半衰期,较低的药物剂量,是其他长效G-CSF的1/3,与公司现有产品特尔津为长短效产品组合。公司已将珮金在中国大陆的独家推广销售权利授权给江苏复星医药,已获得7300万元人民币的首付款和里程碑款项,复星强大的商业化能力有望助力珮金快速放量。
3.2长效生长激素市场空间广阔,公司产品有望国内第二家上市
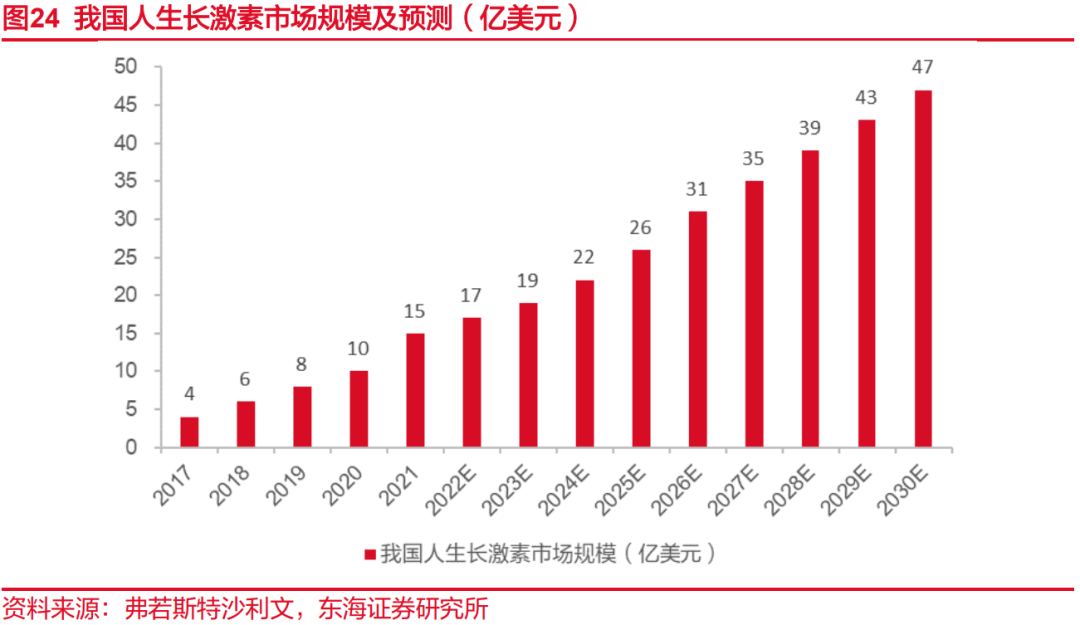
我国生长激素市场空间大。生长激素是由人体脑垂体前叶分泌的一种肽类激素,能促进骨骼、内脏和全身生长,促进蛋白质合成,影响脂肪和矿物质代谢,在人体生长发育中起着关键性作用。通常情况,主要用于治疗与生长激素缺乏有关的疾病和身材矮小症以及用于重度烧伤等治疗领域。据弗若斯特沙利文数据,2017-2021年,我国儿童生长激素缺乏症的治疗市场规模由4亿美元增长至15亿美元,年复合增长率为30.26%,预计2025年增至26亿美元,到2030年将达到47亿美元,维持快速增长态势。
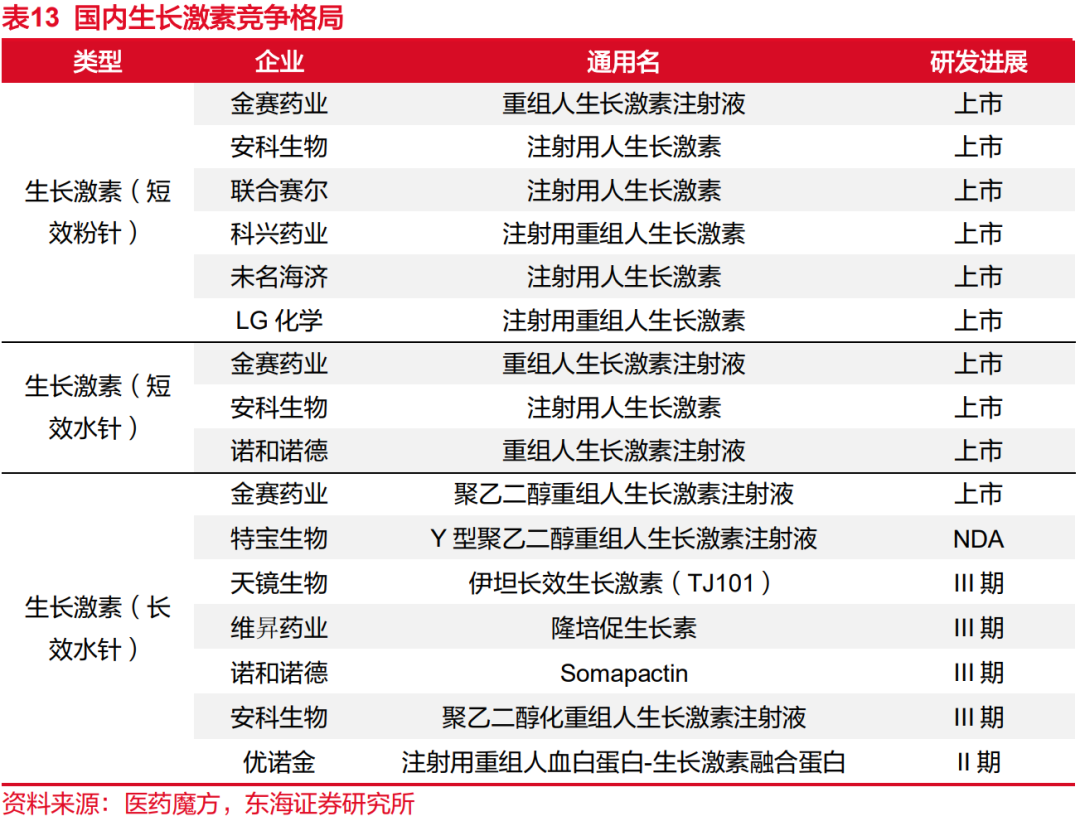
公司长效生长激素有望成为国内第二款上市产品。目前国内获批的生长激素按类型划分可分为短效生长激素粉针剂(粉针、水针)和长效生长激素水针剂(水针)。长效水针作为新剂型,在提高患者接受度、耐受性及治疗灵活性方面比短效生长激素疗法具有潜在优势。在我国,生长激素赛道呈现一家独大的局面,长春高新旗下的金赛药业是国内最早、规模最大的生长激素药企,且实现三种剂型全部上市。目前,国内实现短效粉针剂型上市的企业有6家:金赛药业、安科生物、科兴药业、未名海济、联合赛尔、LG化学,竞争不充分;实现短效水针剂型上市的企业有3家:金赛药业、安科生物、诺和诺德;实现长效水针剂型上市的有金赛药业1家,公司的长效生长激素YPEG-GH已于2024年1月上市申请获得受理,采用40kD Y型分支聚乙二醇修饰,在保证疗效及安全性的前提下,较短效生长激素进一步降低总给药剂量,以获得更佳的长期药物安全及有效性,有望成为国内第二家上市长效生长激素产品。
3.3长效促红素研发进展靠前
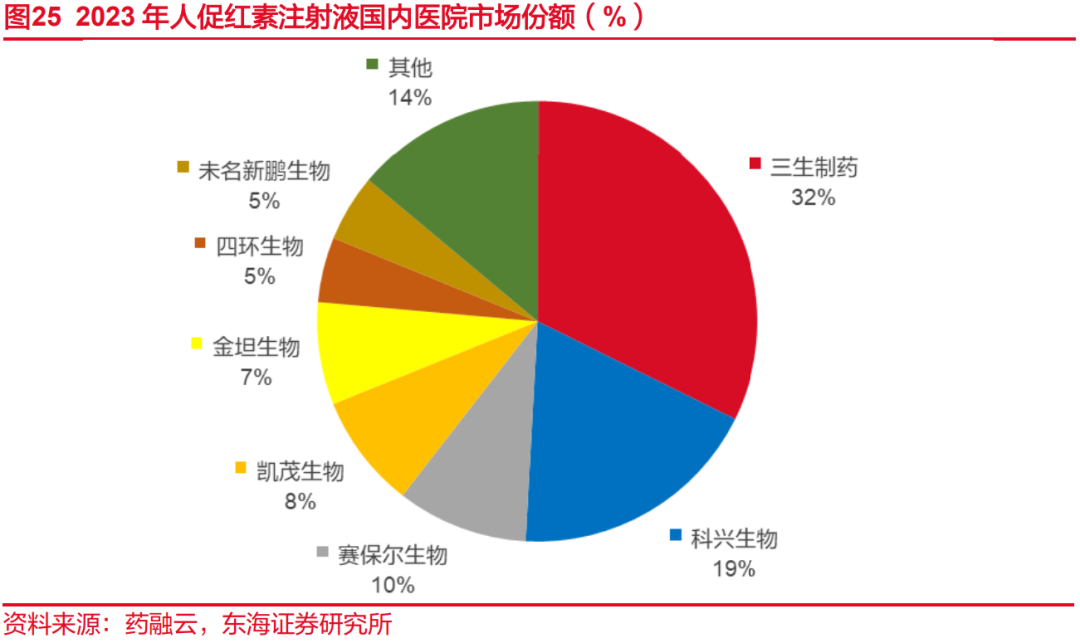
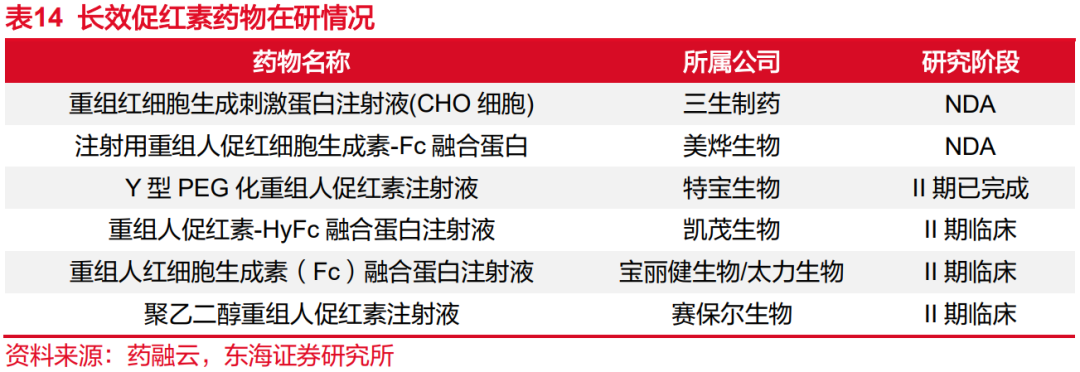
人促红素EPO是一种调节红细胞生成的细胞因子,临床主要作为肾功能不全、化疗和围术期贫血的一线治疗用药。目前,重组人促红素注射液国内上市产品厂商有10余家,竞争相对较为激烈,国内重组人促红素主要厂商包括三生制药、科兴生物、赛保尔生物、凯茂生物、金坦生物、四环生物等。公司长效EPO目前已完成临床II期,准备开展临床III期研究,目前国内进度仅次于三生制药和美烨生物。
▌4.盈利预测
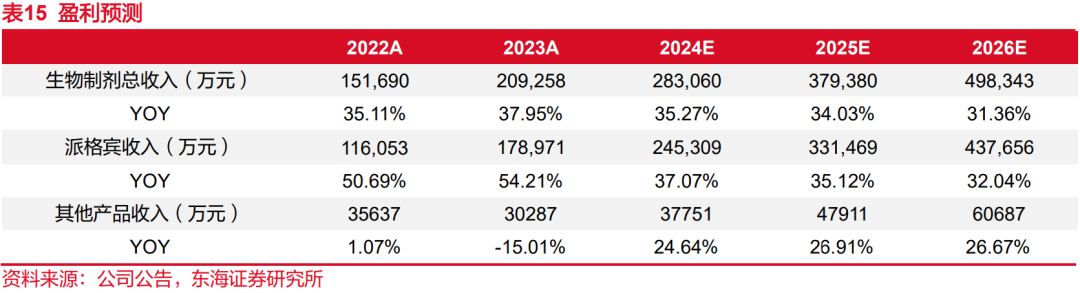
公司主营产品可分为两大类,一、用于病毒性肝炎领域的派格宾,二、用于肿瘤放化疗后血细胞减少的重组蛋白产品,针对两类产品做出以下假设和预测:
派格宾:派格宾主要用于慢性乙肝患者的治疗,我国慢性乙肝患者人数近3000万,存在巨大的治疗需求。派格宾作为目前唯一一款长效干扰素α产品,具备良好竞争优势。公司正在开展慢性乙型肝炎临床治愈研究,为派格宾提供更多临床数据。我们假设2024-2026年派格宾营收同比增速分别为37.07%/35.12%/32.04%。
其他产品:公司其他产品包括成熟产品特尔津、特尔康、特尔立和2023年新上市产品珮金,以上产品主要用于肿瘤患者放化疗后的中性粒细胞、血小板、白细胞的减少,产品销售情况与肿瘤放化疗人数、医院就诊率等密切相关,其中珮金为新上市的长效制剂,有望实现快速放量。公司长效生长激素的上市申请已获受理,预计2025年上市。我们预计2024-2026年其他类产品营收同比增速分别为24.64%/26.91%/26.67%。
▌5.投资建议
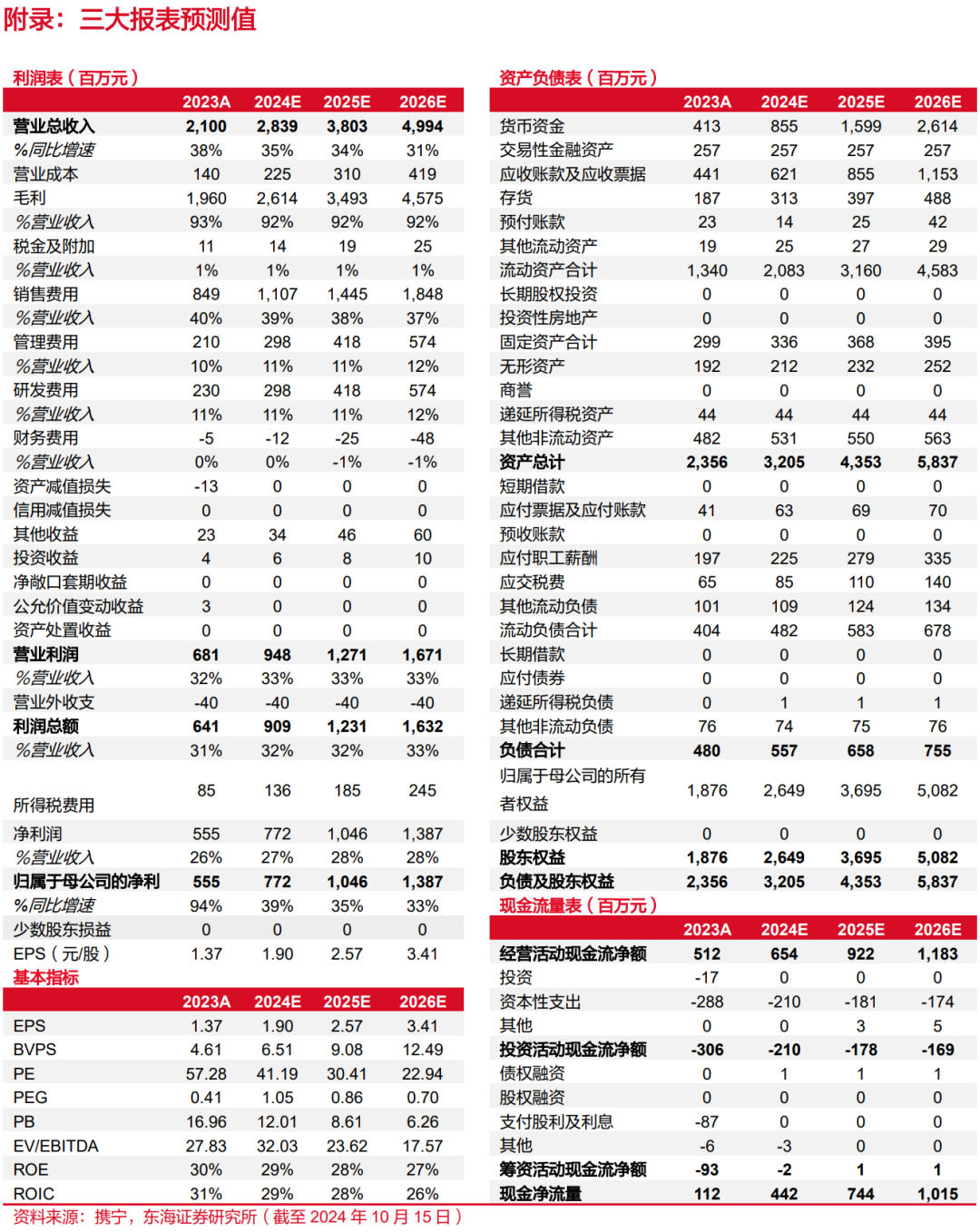
公司核心产品持续放量,我们预计公司2024-2026年实现营收28.39/38.03/49.94亿元,实现归母净利润7.72/10.46/13.87亿元,对应EPS分别为1.90/2.57/3.41,对应PE分别为41.19/30.41/22.94倍。维持“买入”评级。
▌6.风险提示
行业政策变动风险:随着医药卫生体制改革深入推进,带量采购、医保支付方式改革等政策落地实施,公司产品存在价格下降风险;
产品商业化不及预期风险:派格宾是公司主要产品,若慢性乙肝临床治愈理念深入速度不及预期或联合治疗方案的循证医学证据质量和数量不及预期,可能存在销售不及预期风险;
技术升级迭代风险:若在重组蛋白质药物长效化修饰、蛋白质药物合成等公司核心技术相关领域出现革命性的重大技术发现,公司产品可能受到较大冲击。
// 报告信息 //

证券研究报告:《特宝生物(688278):乙肝临床治愈市场空间广阔,派格宾持续放量可期——公司深度报告》
对外发布时间:2024年10月15日
报告发布机构:东海证券股份有限公司
// 声明 //

一、评级说明:
1.市场指数评级:
2.行业指数评级:
3.公司股票评级:
二、分析师声明:
本报告署名分析师具有中国证券业协会授予的证券投资咨询执业资格并注册为证券分析师,具备专业胜任能力,保证以专业严谨的研究方法和分析逻辑,采用合法合规的数据信息,审慎提出研究结论,独立、客观地出具本报告。
本报告仅供“东海证券股份有限公司”客户、员工及经本公司许可的机构与个人阅读和参考。在任何情况下,本报告中的信息和意见均不构成对任何机构和个人的投资建议,任何形式的保证证券投资收益或者分担证券投资损失的书面或口头承诺均为无效,本公司亦不对任何人因使用本报告中的任何内容所引致的任何损失负任何责任。本公司客户如有任何疑问应当咨询独立财务顾问并独自进行投资判断。
四、资质声明:
东海证券股份有限公司是经中国证监会核准的合法证券经营机构,已经具备证券投资咨询业务资格。我们欢迎社会监督并提醒广大投资者,参与证券相关活动应当审慎选择具有相当资质的证券经营机构,注意防范非法证券活动。